Biokonjugatsiya - Bioconjugation
Biokonjugatsiya otxonani shakllantirishning kimyoviy strategiyasidir kovalent bog'lanish ikkita molekula o'rtasida, ularning kamida bittasi a biomolekula.
Funktsiya
Biyomolekulalarni tushunishdagi so'nggi yutuqlar ularni tibbiyot va materiallar kabi ko'plab sohalarda qo'llashga imkon berdi. Sintetik modifikatsiyalangan biomolekulalar turli xil funktsiyalarga ega bo'lishi mumkin, masalan, uyali hodisalarni kuzatish, ochib berish ferment funktsiyasi, aniqlash oqsil biodistribution, tasvirlash aniq biomarkerlar va etkazib berish giyohvand moddalar maqsadli hujayralarga.[1][2][3][4] Biokonjugatsiya - bu o'zgartirilgan biomolekulalarni boshqalari bilan bog'laydigan hal qiluvchi strategiya substratlar.
Sintez
Sintez biokonjugatlarning oddiy va o'ziga xos bo'lmagan ishlatilishidan tortib turli xil qiyinchiliklarni o'z ichiga oladi lyuminestsent bo'yoq ning murakkab dizayniga marker antikor dori konjugatlari.[1][3] Natijada, turli xil biokonjugatsiya reaktsiyalari - kimyoviy reaktsiyalar ikkita biomolekulani bir-biriga bog'lab qo'yish - oqsillarni kimyoviy o'zgartirish uchun ishlab chiqilgan. Proteinlarda biokonjugatsiya reaktsiyalarining umumiy turlari birlashishdir lizin aminokislotalar qoldiqlari, ulanish sistein qoldiqlar, birikma tirozin qoldiqlari, modifikatsiyasi triptofan qoldiqlari va N- va C - terminal.[1][3][4]
Biroq, bu reaktsiyalar ko'pincha etishmayapti kimyoviy tanlov va samaradorlik, chunki ular mahalliy aminokislota qoldiqlari mavjudligiga bog'liq bo'lib, ular odatda selektivlikka to'sqinlik qiladigan juda ko'p miqdorda mavjud. Sintetik molekulalarni maxsus ravishda oqsillarga biriktira oladigan kimyoviy strategiyalarga ehtiyoj ortib bormoqda. Bitta strategiya - avvalo noyob o'rnatish funktsional guruh oqsilga, so'ngra a bioorthogonal yoki bosish turi Ushbu noyob funktsional guruh bilan biomolekulani birlashtirish uchun reaktsiya qo'llaniladi.[1] Mahalliy bo'lmagan funktsional guruhlarga qaratilgan bioorthogonal reaktsiyalar biokonjugatsiya kimyosida keng qo'llaniladi. Ba'zi muhim reaktsiyalar modifikatsiyadir keton va aldegidlar, Staudingerni bog'lash bilan azidlar, mis katalizlangan Huisgen cycloaddition azidlar va shtammlar azidlarning Gyussgen sikloturlanishiga yordam berdi.[5][6][7][8]
Oddiy biokonjugatsiya reaktsiyalari
Eng keng tarqalgan biokonjugatsiyalar bu kichik molekulaning birikishi (masalan biotin yoki lyuminestsent bo'yoq) oqsilga yoki oqsil-oqsil konjugatsiyasiga, masalan, antikorning ferment bilan birikishiga.[9] Biyokonjugatsiyada ishlatiladigan boshqa kamroq tarqalgan molekulalar oligosakkaridlar, nuklein kislotalar, sintetik polimerlar kabi polietilen glikol,[10] va uglerodli nanotubalar.[11] Antikor-dori konjugatlari kabi Brentuximab vedotin va Gemtuzumab ozogamitsin shuningdek, biokonjugatsiyaning namunalari bo'lib, farmatsevtika sanoatida faol tadqiqot yo'nalishi hisoblanadi.[12] So'nggi paytlarda biokonjugatsiya ham muhim ahamiyat kasb etmoqda nanotexnologiya bioconjugated kabi dasturlar kvant nuqtalari.
Lizin qoldiqlarining reaktsiyalari
The nukleofil lizin qoldig'i, odatda oqsil biokonjugatsiyasida odatda maqsadli joy omin - reaktiv N-gidroksisuktsinimidil (NHS) Esterlar.[3] Eng maqbul sonini olish uchun deprotatsiya qilingan lizin qoldiqlari, pH ning suvli eritma ning ostida bo'lishi kerak pKa lizin ammoniy 10,5 atrofida bo'lgan guruh, shuning uchun reaksiyaning odatdagi pH qiymati taxminan 8 va 9 ni tashkil qiladi. Ulanish reaksiyasi uchun umumiy reagent NHS-esterdir (quyidagi birinchi reaktsiyada ko'rsatilgan Shakl 1), bu lizin orqali nukleofil lizin bilan reaksiyaga kirishadi asilatsiya mexanizm. Shunga o'xshash boshqa reaktivlar izosiyanatlar va izotiyosiyanatlar shunga o'xshash mexanizmga ega bo'lgan (ikkinchi va uchinchi reaktsiyalarda ko'rsatilgan Shakl 1 quyida).[1] Benzoil ftoridlar (quyida keltirilgan oxirgi reaktsiyada ko'rsatilgan Shakl 1), bu oqsillarni lizinli modifikatsiyasini yumshoq sharoitlarda (past harorat, fiziologik) o'zgartirishga imkon beradi pH ), yaqinda klassik ishlatiladigan lizinga xos reagentlarga alternativ sifatida taklif qilingan.[13]

Sistein qoldiqlarining reaktsiyalari
Erkin sistein kamdan-kam hollarda oqsil yuzasida paydo bo'lganligi sababli, bu xoselektiv modifikatsiya qilish uchun juda yaxshi tanlovdir.[14] Asosiy sharoitda sistein qoldiqlari a hosil qilish uchun deprotatsiya qilinadi tiolat yumshoq bilan reaksiyaga kirishadigan nukleofil elektrofillar, kabi maleimidlar va yodoatsetamidlar (dastlabki ikki reaktsiyada ko'rsatilgan Shakl 2 quyida). Natijada, a uglerod-oltingugurt aloqasi hosil bo'ladi. Sistein qoldiqlarining yana bir modifikatsiyasi hosil bo'lishini o'z ichiga oladi disulfid birikmasi (uchinchi reaktsiyada ko'rsatilgan Shakl 2). The kamaytirilgan sistein qoldiqlari bilan reaksiyaga kirishadi ekzogen disulfidlar, oqsilda yangi disulfid bog'lanishini hosil qiladi. Reaktsiyani qo'zg'atish uchun ko'pincha disulfidlarning ko'pi ishlatiladi, masalan, 2-tiopiridon va 3-karboksi-4-nitriofenol.[1][3] Elektron etishmasligi alkinlar boshqa nukleofil aminokislota qoldiqlari ishtirokida oqsillarning sistein qoldiqlari bilan selektiv reaksiya ko'rsatgani namoyish etildi. Alkin o'rnini bosishiga qarab, bu reaksiyalar ajralishi mumkin (alkinon hosilalari ishlatilganda),[15] yoki gidrolitik jihatdan barqaror biokonjugatlar (qachon 3-arilpropiolonitril ishlatiladi; Quyidagi so'nggi reaktsiya Shakl 2).[16]

Tirozin qoldiqlarining reaktsiyalari
Tirozin qoldiqlari nisbatan reaktiv emas; shuning uchun ular biokonjugatsiya uchun mashhur maqsad bo'lmagan. So'nggi rivojlanish tirozinni o'zgartirish mumkinligini ko'rsatdi elektrofil aromatik almashtirishlar (EAS) reaktsiyalari va ular uchun tanlangan aromatik ga qo'shni bo'lgan uglerod fenolik gidroksil guruh.[1] Bu, ayniqsa, sistein qoldiqlarini aniqlab bo'lmaydigan holatlarda juda foydali bo'ladi. Xususan, diazonium samarali juftliklar tirozin qoldiqlari bilan (diazonyum tuzi da birinchi reaksiyada reaktiv sifatida ko'rsatilgan Shakl 3 quyida) va an elektron chiqaradigan substituent diazonium tuzining 4-pozitsiyasida reaksiya samaradorligini samarali oshirishi mumkin. Shunga o'xshash tsiklik diazodikarboksamid hosilasi 4-fenil-1,2,4-triazol-3,5-dion (PTAD) tirozin qoldiqlarida selektiv biokonjugatsiya (ikkinchi reaktsiya Shakl 3 quyida).[17] Uch komponentli Mannich tipidagi reaktsiya bilan aldegidlar va anilinalar (oxirgi reaktsiya Shakl 3) shuningdek, engil optimallashtirilgan reaktsiya sharoitida nisbatan tirozin-selektiv deb ta'riflangan.[18]

N va C terminalarining reaktsiyalari
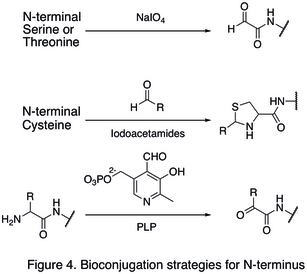
Tabiiy aminokislota qoldiqlari odatda ko'p miqdorda mavjud bo'lganligi sababli, bitta saytni o'zgartirish ko'pincha qiyin bo'ladi. Protein terminiga yo'naltirilgan strategiyalar ishlab chiqilgan, chunki ular oqsil modifikatsiyasining sayt selektivligini sezilarli darajada oshirgan. N-termini modifikatsiyalaridan biri quyidagilarni o'z ichiga oladi funktsionalizatsiya terminal aminokislota. The oksidlanish N-terminal serin va treonin qoldiqlari keyingi bioortogonal reaktsiyalarga kirishishi mumkin bo'lgan N-terminal aldegid hosil qilishga qodir (birinchi reaktsiyada ko'rsatilgan Shakl 4). Modifikatsiyaning yana bir turi quyidagilarni o'z ichiga oladi kondensatsiya ishlab chiqaruvchi aldegid bilan N-terminal sistein tiazolidin yuqori pH darajasida barqaror (ikkinchi reaktsiya in Shakl 4). Foydalanish piridoksal fosfat (PLP), bir nechta N-terminalli aminokislotalarga duch kelishi mumkin transaminatsiya N-terminalni berish aldegid, kabi glitsin va aspartik kislota (uchinchi reaktsiya Shakl 4).
C-termini modifikatsiyasining misoli mahalliy kimyoviy ligatsiya (NCL), bu C-terminali orasidagi birikma tioester va N-terminal sistein (Shakl 5).

Bioorthogonal reaktsiyalar
Ketonlar va aldegidlarning modifikatsiyasi
Keton yoki aldegidni oqsilga N-terminalli serin qoldiqlarini oksidlanishi yoki PLP bilan transaminatsiya qilish orqali biriktirish mumkin. Bundan tashqari, ular qo'shilish orqali kiritilishi mumkin tabiiy bo'lmagan aminokislotalar orqali Tirrell usuli yoki Shultz usuli.[5] Keyin ular tanlab alkoksiamin va a bilan zichlashadi gidrazin, ishlab chiqarish oksim va gidrazon hosilalar (birinchi va ikkinchi reaktsiyalarda, navbati bilan, ko'rsatilgan 6-rasm). Ushbu reaktsiya oqsillarni biokonjugatsiyasi jihatidan juda xemoselektiv, ammo reaktsiya tezligi sekin. Mexanik tadqiqotlar shuni ko'rsatadiki stavkani aniqlash bosqichi bo'ladi suvsizlanish ning tetraedral oraliq, shuning uchun yumshoq kislotali degidratatsiya bosqichini tezlashtirish uchun ko'pincha eritma ishlatiladi.[2]

Nukleofil katalizatorning kiritilishi reaktsiya tezligini sezilarli darajada oshirishi mumkin (ko'rsatilgan Shakl 7). Masalan, foydalanish anilin nukleofil katalizator sifatida, kamroq protonlangan karbonil aholisi juda ko'p bo'lgan protonlangan holga keladi Shiff bazasi.[19] Boshqacha qilib aytganda, u yuqori konsentratsiyali reaktiv elektrofil hosil qiladi. Keyinchalik oksim ligasi tezda yuzaga kelishi mumkin va engil kislotali sharoitda bu ko'rsatkich 400 baravargacha ko'tarilganligi haqida xabar berilgan.[19] Ushbu katalizatorning kaliti shundaki, u kerakli mahsulot bilan raqobatlashmasdan reaktiv elektrofil hosil qilishi mumkin.

Proksimal funktsional guruhlardan foydalanadigan so'nggi o'zgarishlar gidrazon kondensatsiyasini ta'minladi[20] 20 M da ishlash−1s−1 500-10000 M gacha davom etadigan oksim kondansatsiyalari aniqlanganda neytral pH da−1s−1 qo'shilgan katalizatorlarsiz neytral pH da.[21][22]
Azidlar bilan staudinger bog'lash
The Staudingerni bog'lash azidlar va fosfin kimyoviy biologiya sohasida keng qo'llanilgan. Chunki u otxonani shakllantirishga qodir amid bog'i tirik hujayralar va hayvonlarda bu modifikatsiyaga tatbiq etilgan hujayra membranasi, jonli ravishda tasvirlash va boshqa biokonjugatsiya tadqiqotlari.[23][24][25][26]
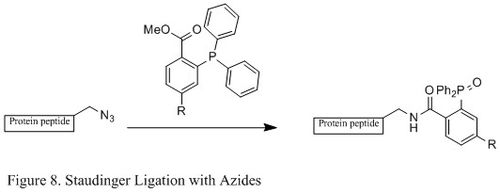
Klassik Staudinger reaktsiyasidan farqli o'laroq, Staudingerni bog'lash a ikkinchi darajali reaktsiya unda stavkani cheklovchi qadam shakllanishi fosfazid (ko'rsatilgan maxsus reaktsiya mexanizmi 9-rasm). The trifenilfosfin avval azid bilan reaksiyaga kirishib, to'rt a'zoli halqa orqali azaylid hosil qiladi o'tish holati, keyin esa molekula ichidagi reaktsiya iminofosforan oraliq, keyinchalik gidroliz ostida amid-bog'lanishni ta'minlaydi.[27]

Azidlarning gyussgen siklizatsiyasi
Mis azidlarning Gyussgen siklizatsiyasini kataliz qildi
Azid xemoselektiv oqsillarni modifikatsiyalash uchun mashhur maqsadga aylandi, chunki ular hajmi kichik va qulay termodinamik reaktsiya potentsiali. Bunday azid reaktsiyalaridan biri [3 + 2] bilan sikloiddition reaksiyasidir alkin, ammo reaksiya yuqori haroratni talab qiladi va ko'pincha aralashmalarini beradi regioizomerlar.

Kimyogar tomonidan ishlab chiqilgan takomillashtirilgan reaktsiya Karl Barri Sharpless mis (I) katalizatorini o'z ichiga oladi, bu esa azidni terminal alkin bilan biriktiradi, ular faqat 1,4 o'rnini bosadigan 1,2,3 triazollarni yuqori rentabellikda beradi (quyida ko'rsatilgan Shakl 11). Mexanik tadqiqotlar bosqichma-bosqich reaktsiyani taklif qiladi.[8] Cu (I) birinchi juftliklar bilan atsetilenlar, so'ngra u azid bilan reaksiyaga kirishib, oltita a'zoli oraliq hosil qiladi. Jarayon juda kuchli bo'lib, u pH qiymati 4 dan 12 gacha o'zgarib turadi va mis (II) sulfat ko'pincha katalizator sifatida kamaytiruvchi vosita.[8]

Kuchlanish azidlarning Gyussgen siklizatsiyasini kuchaytirdi
Staudinger ligatsiyasi tirik hujayralarda katta toksikatsiz biokimyoviy birikma bo'lsa ham, fosfinning havo oksidlanishiga sezgirligi va uning zaifligi eruvchanlik suvda uning samaradorligiga sezilarli darajada to'sqinlik qiladi. Mis (I) katalizlangan azid-alkin birikmasi fiziologik sharoitda oqilona reaktsiya tezligi va samaradorligiga ega, ammo mis muhim ahamiyatga ega toksiklik va ba'zida tirik hujayralardagi oqsil funktsiyalariga xalaqit beradi. 2004 yilda kimyogar Kerolin R. Bertozsiniki laboratoriya suzilgan siklootsit va aziddan foydalangan holda metallsiz [3 + 2] siklokladkasini ishlab chiqdi. Eng kichik turg'un sikloalkin bo'lgan siklootsit, azid bilan [3 + 2] siklokompressiya orqali juftlashib, ikkita regioizomerik triazolaga olib keladi (Shakl 12).[6] Reaksiya tezda sodir bo'ladi xona harorati va shuning uchun tirik hujayralarni salbiy ta'sir ko'rsatmasdan samarali o'zgartirish uchun foydalanish mumkin. Shuningdek, o'rnatilishi haqida xabar berilgan ftor tsiklik alkinda o'rinbosarlar reaktsiya tezligini ancha tezlashtirishi mumkin.[2][28]

Amaliy biokonjugatsiya usullariga misollar
O'sish omillari
TGF-b ning temir oksidi nanopartikullariga biokonjugatsiyasi va uning in-vitro magnit gipertermiya orqali faollashishi haqida xabar berilgan.[29] Buning uchun 1- (3-dimetilaminopropil) etilkarbodiimid yordamida N-gidroksisuktsinimid qo'shilib, o'sish faktori bo'yicha erkin birlamchi aminlar bilan birlamchi amid bog'lari hosil bo'ldi. Uglerodli nanotubalar biokonjugatsiya bilan birgalikda TGF-link ni bog'lash uchun muvaffaqiyatli ishlatilib, so'ngra infraqizil nurlari bilan faollashadi.[30] Odatda, bu reaktsiyalar o'zaro bog'liqlikdan foydalanishni o'z ichiga olgan, ammo ularning ba'zilari qiziqish birikmasi va asosiy material o'rtasida molekulyar bo'shliqni qo'shib, o'z navbatida yuqori darajadagi o'ziga xos bo'lmagan bog'lanish va kiruvchi reaktivlikni keltirib chiqaradi.[31]
Shuningdek qarang
- Immunofloresans
- Biyomolekulyar muhandislik
- Biotinilatsiya
- SpyTag / SpyCatcher
- Tabiiy bo'lmagan aminokislotalar
- Biokonjugat kimyosi jurnal
Adabiyotlar
- ^ a b v d e f g Stefanopulos, N .; Frensis, M. B. (2011). "Samarali oqsil biokonjugatsiya strategiyasini tanlash". Tabiat kimyoviy biologiyasi. 7 (12): 876–884. doi:10.1038 / nchembio.720. PMID 22086289.
- ^ a b v Tilli, S.D .; Joshi, N. S .; Frensis, M. B. (2008). "Oqsillar: kimyo va kimyoviy reaktivlik". Wiley Kimyoviy Biologiya Entsiklopediyasi. doi:10.1002 / 9780470048672.wecb493. ISBN 978-0470048672.
- ^ a b v d e Frensis, M. B.; Carrico, I. S. (2010). "Protein biokonjugatsiyasida yangi chegaralar". Kimyoviy biologiyaning hozirgi fikri. 14 (6): 771–773. doi:10.1016 / j.cbpa.2010.11.006. PMID 21112236.
- ^ a b Kalia, J .; Raines, R. T. (2010). "Biokonjugatsiyadagi yutuqlar". Hozirgi organik kimyo. 14 (2): 138–147. doi:10.2174/138527210790069839. PMC 2901115. PMID 20622973.
- ^ a b Karriko, I. S .; Karlson, B. L.; Bertozzi, C. R. (2007). "Genetik kodlangan aldegidlarni oqsillarga kiritish". Tabiat kimyoviy biologiyasi. 3 (6): 321–322. doi:10.1038 / nchembio878. PMID 17450134.
- ^ a b Agard, N. J .; Prescher, J. A .; Bertozzi, C. R. (2004). "Tirik tizimlarda biomolekulalarning kovalent modifikatsiyasi uchun azim-alkin siklidroduksiyasi". Amerika Kimyo Jamiyati jurnali. 126 (46): 15046–15047. doi:10.1021 / ja044996f. PMID 15547999.
- ^ Kolb, H. C .; Finn, M. G.; Sharpless, K. B. (2001). "Chemical-ni bosing: bir nechta yaxshi reaktsiyalarning xilma-xil kimyoviy funktsiyasi". Angewandte Chemie International Edition. 40 (11): 2004–2021. doi:10.1002 / 1521-3773 (20010601) 40:11 <2004 :: AID-ANIE2004> 3.0.CO; 2-5. PMID 11433435.
- ^ a b v Rostovtsev, Vsevolod V.; Yashil, Lyuk G.; Fokin, Valeriy V.; Sharpless, K. Barri (2002). "A Stepwise Huisgen Cycloaddition Process: Mis (I) -Katalized Regioselective" ligation "of Azides and Terminal Alkines" ". Angewandte Chemie International Edition. 41 (14): 2596–2599. doi:10.1002 / 1521-3773 (20020715) 41:14 <2596 :: AID-ANIE2596> 3.0.CO; 2-4. ISSN 1433-7851. PMID 12203546.
- ^ Koniev, O .; Vagner, A. (2015). "Biokonjugatsiya uchun endogen aminokislota selektiv bog'lanish hosil qilish reaktsiyalari sohasidagi o'zgarishlar va so'nggi yutuqlar". Kimyoviy. Soc. Vah. 44 (15): 5495–5551. doi:10.1039 / C5CS00048C. PMID 26000775.
- ^ Thordarson, P.; Le Droumaguet, B.; Velonia, K. (2006). "Protein-polimer konjugatlari aniq sintezi va potentsial qo'llanilishi". Amaliy mikrobiologiya va biotexnologiya. 73 (2): 243–254. doi:10.1007 / s00253-006-0574-4. PMID 17061132. S2CID 23657616.
- ^ Yang, V.; Thordarson, P. (2007). "Biologik va biomedikal dasturlar uchun uglerodli nanotubalar". Nanotexnologiya. 18 (41): 412001. Bibcode:2007Nanot..18O2001Y. doi:10.1088/0957-4484/18/41/412001.
- ^ Gerber, HP; Senter, PD; Grewal, IS (2009). "Antikorli dori-konjugatlar o'simta tomirlarini yo'naltirish: hozirgi va kelajakdagi rivojlanish". MAb. 1 (3): 247–53. doi:10.4161 / mabs.1.3.8515. PMC 2726597. PMID 20069754. Arxivlandi asl nusxasi 2014 yil 2 fevralda.
- ^ Dovgan, I .; Ursuegui, S .; Erb, S .; Mishel, C .; Kolodych, S .; Sianferani, S .; Vagner, A. (2017). "Asil Fluoridlar: Plug-and-Play strategiyasi orqali tez, samarali va ko'p qirrali lizinga asoslangan oqsil birikmasi". Biokonjugat kimyoviy moddasi. 28 (5): 1452–1457. doi:10.1021 / acs.bioconjchem.7b00141. PMID 28443656.
- ^ Fodje, M. N .; Al-Karadagi, S. (2002). "G-spirali uchun paydo bo'lishi, konformatsion xususiyatlari va aminokislotalarga moyilligi". Protein Eng. 15 (5): 353–358. doi:10.1093 / protein / 15.5.353. PMID 12034854.
- ^ Shiu, H.-Y .; Chan, T.-C .; Xo, C.-M .; Lin, Y .; Vong, M.-K .; Che, C.-M. (2009). "Suvli muhitda sistein tarkibidagi peptidlarni modifikatsiyalash uchun ajraladigan reaktiv sifatida elektronlar etishmaydigan alkinlar". Kimyoviy. Yevro. J. 15 (15): 3839–3850. doi:10.1002 / chem.200800669. PMID 19229937.
- ^ Koniev, O .; Lerixe, G.; Nothisen M.; Remi, J.-S .; Strub, J.-M .; Sheffer-Reiss, C .; Dorsselaer, A .; Baati, R .; Vagner, A. (2014). "3-arilpropiolonitril bilan sisteinni tanlab qaytarib bo'lmaydigan kimyoviy yorlig'i". Biokonjugat kimyoviy moddasi. 25 (2): 202–206. doi:10.1021 / bc400469d. PMID 24410136.
- ^ Ban, H .; Nagano, M .; Gavrilyuk, J .; Barbas, CF. (2015). "Tirozin orqali yuz va barqaror aloqalar: tirozin-klik reaktsiyasi bilan biokonjugatsiya strategiyalari". Biokonjugat kimyoviy moddasi. 4 (24): 520–532. doi:10.1021 / bc300665t. PMC 3658467. PMID 23534985.
- ^ Joshi, N.S .; Whitaker, L.R .; Frensis, M.B. (2004). "Tanlangan tirozin biokonjugatsiyasi uchun uch komponentli Mannix tipidagi reaktsiya". J. Am. Kimyoviy. Soc. 126 (49): 15942–15943. doi:10.1021 / ja0439017. PMID 15584710.
- ^ a b Dirksen, A .; Xekeng, T. M .; Douson, P. E. (2006). "Oksim ligatsiyasining nukleofil katalizi". Angewandte Chemie International Edition. 45 (45): 7581–4. doi:10.1002 / anie.200602877. PMID 17051631.
- ^ Kool, Erik; Park, Do-Hyoung; Crisalli, Pete (2013). "Tez gidrazonli reaktivlar: elektron va kislota / asos effektlari biologik pH da kuchli ta'sir darajasi". Amerika Kimyo Jamiyati jurnali. 135 (47): 17663–17666. doi:10.1021 / ja407407h. PMC 3874453. PMID 24224646.
- ^ Shmidt, Paskal; Chjou, Linna; Tishinov, Kiril; Zimmermann, Kaspar; Gillingham, Dennis (2014). "Dialdegidlar tsiklik oraliq fazilati bilan neytral pH darajasida juda tez biokonjugatsiyalarga olib keladi". Angewandte Chemie International Edition. 53 (41): 10928–10931. doi:10.1002 / anie.201406132. PMID 25164607.
- ^ Shmidt, Paskal; Stress, Sedrik; Gillingham, Dennis (2015). "Boron kislotalari neytral pH qiymatida oksimning tez kondensatsiyalanishini osonlashtiradi" (PDF). Kimyo fanlari. 6 (6): 3329–3333. doi:10.1039 / C5SC00921A. PMC 5656983. PMID 29142692.
- ^ Lemie, G. A .; De Graffenri, K. L.; Bertozzi, R. R. (2003). "Staudinger ligasi tomonidan faollashtirilgan florogen bo'yoq". Amerika Kimyo Jamiyati jurnali. 125 (16): 4708–4709. doi:10.1021 / ja029013y. PMID 12696879.
- ^ Laughlin, S. T .; Baskin, J. M .; Amaxer, S. L .; Bertozzi, C. R. (2008). "Zebrafish rivojlanishida membrana bilan bog'liq glikanlarning Vivo jonli tasvirida". Ilm-fan. 320 (5876): 664–667. Bibcode:2008 yil ... 320..664L. doi:10.1126 / science.1155106. PMC 2701225. PMID 18451302.
- ^ Sakson, E .; Bertozzi, R. R. (2000). "O'zgartirilgan Staudinger reaktsiyasi bilan hujayra sirtini muhandislik qilish". Ilm-fan. 287 (5460): 2007–2010. Bibcode:2000Sci ... 287.2007S. doi:10.1126 / science.287.5460.2007. PMID 10720325. S2CID 19720277.
- ^ Prescher, J. A .; Dube, D. H .; Bertozzi, C. R. (2004). "Tirik hayvonlarda hujayra sirtini kimyoviy qayta qurish". Tabiat. 430 (7002): 873–877. Bibcode:2004 yil natur.430..873P. doi:10.1038 / tabiat02791. PMID 15318217. S2CID 4371934.
- ^ Lin, F. L .; Xoyt, H. M.; Van Xelbek, X.; Bergman, R. G.; Bertozzi, C. R. (2005). "Staudinger Ligasining mexanik tekshiruvi". Amerika Kimyo Jamiyati jurnali. 127 (8): 2686–2695. doi:10.1021 / ja044461m. PMID 15725026.
- ^ Chang, P. V.; Prescher, J. A .; Sletten, E. M.; Baskin, J. M .; Miller, I. A .; Agard, N. J .; Mana, A .; Bertozzi, R. R. (2010). "Tirik hayvonlarda missiz chertish kimyosi". Milliy fanlar akademiyasi materiallari. 107 (5): 1821–1826. Bibcode:2010PNAS..107.1821C. doi:10.1073 / pnas.0911116107. PMC 2836626. PMID 20080615.
- ^ Azie, O; Grinberg, ZF; Batich, CD; Dobson, JP (2019). "Uzoqdan faollashtirish uchun yashirin transformatsion o'sish omilining karbodiimid konjugatsiyasi β1 superparamagnitik temir oksidi nanozarralariga". Int J Mol Sci. 20 (13): 3190. doi:10.3390 / ijms20133190. PMC 6651417. PMID 31261853.
- ^ Lin, L .; Liu, L .; Chjao, B .; va boshq. (2015). "TGF-b signalizatsiyasini infraqizil nurlari yaqinida uglerodli nanotüp yordamida optik faollashtirish". Tabiat nanotexnologiyasi. 10 (5): 465–471. Bibcode:2015NatNa..10..465L. doi:10.1038 / nnano.2015.28. PMID 25775150.
- ^ Lalli, E .; Sarti, G.; Boi, C. (2018). "Spacer qo'lining membrana yaqinligi xromatografiyasida o'ziga xos bo'lmagan bog'lanishiga ta'siri". MRS Communications. 8 (1): 65–70. doi:10.1557 / mrc.2018.4.
