Nukleofil aromatik almashtirish - Nucleophilic aromatic substitution
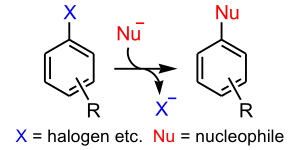
A nukleofil aromatik almashtirish a almashtirish reaktsiyasi yilda organik kimyo unda nukleofil yaxshilikni almashtiradi guruhdan chiqish, masalan haloid, an aromatik halqa. 6 bor nukleofil almashtirish aromatik tizimlarga duch keladigan mexanizmlar:
- The SNAr (qo'shimcha-yo'q qilish) mexanizmi
- xushbo'y SN1 mexanizmi bilan uchrashdi diazonyum tuzlari
- The benzin mexanizm (E1cb-Ad.)N)
Ulardan eng muhimi SNAr mexanizmi, qaerda elektronni tortib oluvchi guruhlar halqani nukleofil hujumiga qarab faollashtiring, masalan, mavjud bo'lsa nitro funktsional guruhlari joylashtirilgan orto yoki paragraf uchun haloid guruhdan chiqish.
SNAr reaksiya mexanizmi
Quyidagi reaktsiya mexanizmi 2,4-dinitroklorobenzolning nukleofil aromatik o'rnini bosishi Asosiy suvdagi eritma.

Ushbu ketma-ketlikda uglerodlar xlorid bilan bog'langan soat 12 da 1 ugleroddan boshlab soat yo'nalishi bo'yicha 1-6 gacha raqamlanadi. Beri nitro guruh nukleofil o'rnini bosuvchi aktivator va meta-direktor bo'lib, u bog'langan benzol uglerodini salbiy zaryadga ega bo'lishiga imkon beradi. In Meysenxaymer kompleksi, ning bog'lanmagan elektronlari karbanion imkon beruvchi aromatik pi tizimiga bog'lanib qoladi ipso bilan vaqtincha bog'lanish uchun uglerod gidroksil guruh (-OH). Kamroq energiya holatiga qaytish uchun gidroksil guruhi yoki xlorid barglari. Qarorda ikkala jarayon ham sodir bo'ladi. Qidiruv mahsulotning ozgina qismi xloridni yo'qotib, mahsulotga aylanadi (2,4-dinitrofenol), qolgan qismi esa reaktivga qaytadi. 2,4-dinitrofenol pastroq energiya holatida bo'lganligi sababli, u reaktivni hosil qilish uchun qaytmaydi, shuning uchun bir muncha vaqt o'tgach, reaktsiya kimyoviy muvozanat bu 2,4-dinitrofenolni afzal ko'radi.
Ning shakllanishi rezonans-stabillashgan Meysenxaymer kompleksi sust, chunki u yuqoriroqda energiya holati ga qaraganda xushbo'y reaktiv. Xloridning yo'qotilishi tezda, chunki halqa yana aromatik bo'ladi. So'nggi yillarda olib borilgan ishlar shuni ko'rsatadiki, ba'zida Meyzengeymer kompleksi har doim ham haqiqiy oraliq emas, balki 'oldingi S S ning o'tish holati bo'lishi mumkin.N2 'jarayoni, ayniqsa elektronlarni chiqarib oluvchi guruhlar tomonidan barqarorlashish juda kuchli bo'lmasa.[1] 2019 yilgi sharh shuni ta'kidlaydiki, bunday "kelishilgan SNAr 'reaktsiyalari ilgari taxmin qilinganidan ko'ra ko'proq tarqalgan.[2]
Aril galogenidlari klassik "orqa tomondan" o'tishi mumkin emas SN2 reaktsiya. Uglerod-halogen aloqasi halqa tekisligida, chunki uglerod atomi trigonal planar geometriyaga ega. Orqa tarafdagi hujum bloklandi va shuning uchun bu reaktsiya mumkin emas.[3] An SN1 reaktsiya mumkin, lekin juda noqulay. Bu qutqaruvsiz yo'qotishni o'z ichiga oladi guruhdan chiqish va aril kationining hosil bo'lishi.[3] Nitro guruhi eng ko'p uchraydigan faollashtiruvchi guruh, boshqa guruhlar esa siyano va asil guruh.[4] Chiqish guruhi halogen yoki sulfid bo'lishi mumkin. O'sish bilan elektr manfiyligi nukleofil hujum uchun reaktsiya tezligi oshadi.[4] Buning sababi shundaki, S uchun stavkani belgilaydigan qadamNAr reaktsiyasi - bu nukleofilning hujumi va keyinchalik aromatik tizimning buzilishi; tezroq jarayon - bu tark etilayotgan guruh yo'qolganidan keyin aromatik tizimni ijobiy isloh qilish. Shunday qilib, S uchun galogen qoldiruvchi guruh qobiliyatiga nisbatan quyidagi naqsh mavjudNAr: F> Cl-Br> I (ya'ni, S uchun kutilgan tomonga teskari tartibN2 reaktsiya). Agar S nuqtai nazaridan qaralsaN2-reaktsiya bu qarama-qarshi bo'lib tuyuladi, chunki C-F aloqasi organik kimyoda eng kuchli hisoblanadi, chunki ftor S uchun eng yaxshi ajralib chiqadigan guruh hisoblanadi.NAr-C bog'lanishining haddan tashqari qutbliligi tufayli. Nukleofillar omin bo'lishi mumkin, alkoksidlar, sulfidlar va barqarorlashdi karbonionlar.[4]
Nukleofil aromatik almashtirish reaktsiyalari
Arenalarda o'rnini bosuvchi ba'zi odatiy reaktsiyalar quyida keltirilgan.
- In Bambergerni qayta qurish N-fenilgidroksilaminlar 4-aminofenollarga qayta joylashadi. Nukleofil suvdir.
- In Sandmeyer reaktsiyasi va Gatterman reaktsiyasi diazonyum tuzlari galogenidlar bilan reaksiyaga kirishadi.
- The Tabassumlarni qayta tashkil etish bu reaksiya turining molekula ichidagi versiyasidir.
Nukleofil aromatik almashtirish faqat arenalar bilan chegaralanmaydi; reaktsiya yanada osonlik bilan amalga oshiriladi heteroarenlar. Piridinlar ga almashtirilganda ayniqsa reaktiv bo'ladi aromatik orto holati yoki aromatik pul holati chunki manfiy zaryad azot holatida samarali delokalizatsiya qilinadi. Klassik reaktsiyalardan biri Chichibabin reaktsiyasi (Aleksey Chichibabin, 1914) bunda piridin kabi gidroksidi-metal amid bilan reaksiyaga kirishadi natriy amid 2-aminopiridin hosil qilish uchun.[5]
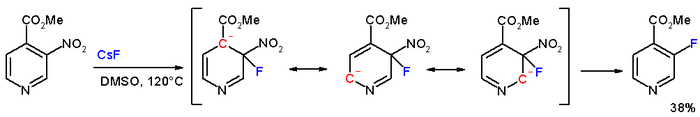
Metil 3-nitropiridin-4-karboksilat birikmasida meta nitro guruhi aslida ko'chirilgan ftor bilan ftorli seziy yilda DMSO 120 ° C da.[6]
Asimmetrik nukleofil aromatik almashtirish
1,3-dikarbonil birikmalari kabi uglerod nukleofillari bilan reaktsiya assimetrik sintez chiral molekulalarining[7] Birinchi marta 2005 yilda xabar berilgan organokatalizator (a bilan ikki tomonlama rolda fazali uzatish katalizatori ) dan olingan xinhonidin (benzillangan N va O da).
Shuningdek qarang
- Elektrofil aromatik almashtirish
- Nukleofil
- O'zgartirish reaktsiyasi
- SN1 reaktsiyasi
- SN2 reaktsiyasi
- SNi reaktsiyasi
- Nukleofil alifatik almashtirish
- Nukleofil asilni almashtirish
Adabiyotlar
- ^ Neumann CN, Hooker JM, Ritter T (iyun 2016). "(19) F (-) va (18) F (-) bilan kontsentrlangan nukleofil aromatik almashtirish". Tabiat. 534 (7607): 369–73. doi:10.1038 / tabiat17667. PMC 4911285. PMID 27281221.
- ^ Rohrbach S, Smit AJ, Pang JH, Puul DL, Tuttle T, Chiba S, Merfi JA (Noyabr 2019). "Konsentrlangan nukleofil aromatik almashtirish reaktsiyalari". Angewandte Chemie. 58 (46): 16368–16388. doi:10.1002 / anie.201902216. PMC 6899550. PMID 30990931.
- ^ a b Kleyden J. Organik kimyo. Oksford universiteti matbuoti.
- ^ a b v Goldstein SW, Bill A, Dhuguru J, Ghoneim O (sentyabr 2017). "Nukleofil aromatik almashtirish" Amin qo'shilishi va uni aniqlash ". Kimyoviy ta'lim jurnali. 94 (9): 1388–90. Bibcode:2017JChEd..94.1388G. doi:10.1021 / acs.jchemed.6b00680.
- ^ Mart J (1966). Ilg'or organik kimyo, reaktsiyalar, mexanizmlar va tuzilish (3-nashr). ISBN 0-471-85472-7.
- ^ Tjosaas F, Fiksdahl A (2006 yil fevral). "Metil 3-floropiridin-4-karboksilatga nukleofil aromatik o'rnini bosuvchi oddiy sintetik yo'l". Molekulalar (Bazel, Shveytsariya). 11 (2): 130–3. doi:10.3390/11020130. PMC 6148553. PMID 17962783.
- ^ Bella M, Kobbelgaard S, Yorgensen KA (2005 yil mart). "Organokatalitik regio- va assimetrik C-selektiv S (N) Ar reaktsiyalari-optik faol spiro-pirrolidon-3,3'-oksoindollarning stereoselektiv sintezi". Amerika Kimyo Jamiyati jurnali. 127 (11): 3670–1. doi:10.1021 / ja050200g. PMID 15771481.




