Merkuriy (II) nitrat - Mercury(II) nitrate
 | |
| Ismlar | |
|---|---|
| IUPAC nomlari Merkuriy dinitrat Merkuriy (II) nitrat | |
| Boshqa ismlar Mercuric nitrat | |
| Identifikatorlar | |
| |
3D model (JSmol ) | |
| ChemSpider | |
| ECHA ma'lumot kartasi | 100.030.126 |
| EC raqami |
|
PubChem CID | |
| RTECS raqami |
|
| UNII | |
| BMT raqami | 1625 |
CompTox boshqaruv paneli (EPA) | |
| |
| |
| Xususiyatlari | |
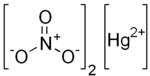
| Hg (YO'Q3)2 | |
| Molyar massa | 324,60 g / mol (suvsiz) |
| Tashqi ko'rinish | rangsiz kristallar yoki oq kukun |
| Hidi | o'tkir |
| Zichlik | 4,3 g / sm3 (monohidrat) |
| Erish nuqtasi | 79 ° C (174 ° F; 352 K) (monohidrat) |
| eriydi | |
| Eriydiganlik | ichida eriydi azot kislotasi, aseton, ammiak ichida erimaydi spirtli ichimliklar |
| −74.0·10−6 sm3/ mol | |
| Xavf | |
| Xavfsizlik ma'lumotlari varaqasi | ICSC 0980 |
| Juda zaharli (T +) Atrof muhit uchun xavfli (N) | |
| R-iboralar (eskirgan) | R26 / 27/28, R33, R50 / 53 |
| S-iboralar (eskirgan) | (S1 / 2), S13, S28, S45, S60, S61 |
| NFPA 704 (olov olmos) | |
| o't olish nuqtasi | Yonuvchan emas |
| Tegishli birikmalar | |
Boshqalar anionlar | Merkuriy (II) sulfat Merkuriy (II) xlorid |
Boshqalar kationlar | Sink nitrat Kadmiy nitrat |
Tegishli birikmalar | Merkuriy (I) nitrat |
Boshqacha ko'rsatilmagan hollar bundan mustasno, ulardagi materiallar uchun ma'lumotlar berilgan standart holat (25 ° C [77 ° F], 100 kPa da). | |
| Infobox ma'lumotnomalari | |
Merkuriy (II) nitrat zaharli rangsiz yoki oq rangga ega eriydi kristalli simob (II) tuz ning azot kislotasi. Bu davolash uchun ishlatilgan mo'yna qilish his qildim "deb nomlangan jarayondaqirg'in qilish '. Iborashlyapa kabi aqldan ozgan 'simob (II) nitratga haddan tashqari ta'sir qilish natijasida kelib chiqqan psixologik kasallik bilan bog'liq. Amaliyot AQShda 1941 yil dekabrda taqiqlanmaguncha davom etdi Amerika Qo'shma Shtatlarining sog'liqni saqlash xizmati. Garchi bu sog'liq uchun foydali bo'lsa-da, taqiq aslida simob (II) nitratini o'sha paytda davom etayotgan urushda detonatorlar ishlab chiqarishda ishlatish uchun ozod qildi.[1]
Ishlab chiqarish
Merkuriy (II) nitrat issiq konsentratsiyali reaksiyaga kirishish yo'li bilan olinadi azot kislotasi bilan simob metall, bu sharoitda nitrat kislota an oksidlovchi vosita. Suyultirilgan azot kislotasi hosil bo'ladi simob (I) nitrat.
Foydalanadi
Merkuriy nitrat simulyatsiya reaktsiyalarida ishlatiladi. Xususan, u ketonlar bilan bog'liq reaktsiyalarda qo'llaniladi. U eng samarali bo'lgan kimyoviy moddalardan biri bu aseton. Ushbu reaktsiyada asetonni o'zgartirish uchun simob nitrat, simob oksidi va kaltsiy sulfat ishlatiladi, bu CH3C (O) CH3, CH ga3C (O) CH2Simob ustuni. Atseton - bu boshqa ko'p miqdordagi simulyatsiya usullari samarasiz bo'lgan birikma.[2] Simob nitrat birikmasi ishlaydi, chunki u kuchli oksidlovchi moddadir.[3] Bundan tashqari, simob nitrat kislotada eritilganda simob nitratning kislota shakli hosil bo'ladi.[4] Kislota shakli saxaroza molekulalarini teskari aylantirishga qodir.[5]
Sog'liqni saqlash haqida ma'lumot
Merkuriy nitrat tanaga Hg kabi ta'sir qiladi2+, bu noorganik simobning bir shakli deb hisoblanadi. Anorganik simob shakllarini turli xil sharoitlarda, shu jumladan terini yorituvchi kremda topish mumkin. Agar noorganik simob yutilsa, u tanadagi muhim oqsillarning tuzilishini o'zgartirishi mumkin. Agar u tuproqqa tushsa, u so'rilishi mumkin va o'simliklar tomonidan qabul qilinishi kerak.[6] Zaharlanishdan aziyat chekadiganlar gijjalar va diareyani dastlabki alomatlari deb bilishadi.[3]
Reaktivlik
Simobli nitrat yonuvchan bo'lmasa-da, u olovni tezlashtirishi mumkin, chunki u oksidlovchi vazifasini bajaradi. Bundan tashqari, u spirtli ichimliklar bilan birlashganda portlovchi birikmalar hosil qilishi mumkin.[7]
Shuningdek qarang
Adabiyotlar
- ^ "Aqldan ozgan shlyapa: Merkuriyning kasbiy xavfi".
- ^ Morton, Avery A.; Penner, Hellmut P. (1951). "Ketonlar va boshqa ba'zi birikmalarning Merkuriy nitrat bilan merkuratsiyasi". Amerika Kimyo Jamiyati jurnali. 73 (7): 3300–3304. doi:10.1021 / ja01151a091.
- ^ a b "Merkuriy nitrat".
- ^ Blyt, Aleksandr Vynter; Blyth, Meredith Wynter (1903). Ovqatlar: ularning kompostatsiyasi va tahlili.
- ^ Cochran, C. B. (1907). "Kislota Mercuric nitrat tomonidan sukrozning inversiyasi". Amerika Kimyo Jamiyati jurnali. 29 (4): 555–556. doi:10.1021 / ja01958a016.
- ^ "Elementar simob va noorganik simob aralashmalari: inson salomatligi aspektlari" (PDF).
- ^ "Merkuriy nitrat".
Tashqi havolalar
- ATSDR - Toksik moddalar portali - Merkuriy (11/14/2013)
- ATSDR - Sog'liqni saqlash bo'yicha bayonot: Merkuriy (11/14/2013)
- ATSDR - ogohlantirish! Metall simob ta'sir qilish naqshlari, 6/26/97 (havola kuzatilishi mumkin emas 14.11.2013)
- ATSDR - Merkuriy uchun tibbiy boshqaruv bo'yicha ko'rsatmalar (11/14/2013)
- ATSDR - Toksikologik profil: Merkuriy (11/14/2013)
- Xavfsizlik ma'lumotlari (MSDS) (havola kuzatilishi mumkin emas 14.11.2013)
- Mercuric nitrat (ICSC)
- Merkuriy
- Merkuriy haqida ma'lumot to'plamlari
- Qanday qilib yaxshi simob elektr aloqalarini o'rnatish kerak, Ommabop fan oylik, 1919 yil fevral, raqamsiz sahifa, Google Books tomonidan skaner qilingan: https://books.google.com/books?id=7igDAAAAMBAJ&pg=PT14

