Diizobutilaluminium gidrid - Diisobutylaluminium hydride
 | |
 | |
| Ismlar | |
|---|---|
| IUPAC nomi Diizobutilaluminiy gidrid | |
| Boshqa ismlar DIBAH; DIBAL; DiBAlH; DIBAL-H; DIBALH | |
| Identifikatorlar | |
3D model (JSmol ) | |
| ChemSpider | |
| ECHA ma'lumot kartasi | 100.013.391 |
| EC raqami |
|
PubChem CID | |
| UNII | |
CompTox boshqaruv paneli (EPA) | |
| |
| |
| Xususiyatlari | |
| C8H19Al (monomer) C16H38Al2 (dimer) | |
| Molyar massa | 142,22 g / mol (monomer) 284,44 g / mol (dimer) |
| Tashqi ko'rinish | Rangsiz suyuqlik |
| Zichlik | 0,798 g / sm3 |
| Erish nuqtasi | -80 ° C (-112 ° F; 193 K) |
| Qaynatish nuqtasi | 1 mm Hg da 116 dan 118 ° C gacha (241 dan 244 ° F; 389 dan 391 K gacha) |
| Zo'ravonlik bilan suv bilan reaksiyaga kirishadi | |
| Eriydiganlik uglevodorod erituvchilarida | Eriydi |
| Xavf | |
| Asosiy xavf | havoda yonadi |
| GHS piktogrammalari |   |
| GHS signal so'zi | Xavfli |
| H220, H225, H250, H260, H314, H318 | |
| P210, P222, P223, P231 + 232, P233, P240, P241, P242, P243, P260, P264, P280, P301 + 330 + 331, P302 + 334, P303 + 361 + 353, P304 + 340, P305 + 351 + 338, P310, P321, P335 + 334, P363, P370 + 378, P377, P381, P402 + 404 | |
Boshqacha ko'rsatilmagan hollar bundan mustasno, ulardagi materiallar uchun ma'lumotlar keltirilgan standart holat (25 ° C [77 ° F], 100 kPa da). | |
| Infobox ma'lumotnomalari | |
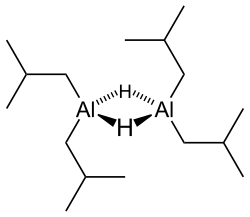
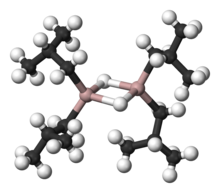
Diizobutilaluminium gidrid (DIBALH, DIBAL, DIBAL-H yoki DIBAH, /ˈdaɪbæl/ DY-bal ) a kamaytiruvchi vosita bilan formula (men-Bu2AlH)2, qayerda men-Bu ifodalaydi izobutil (-CH2CH (CH3)2). Bu organoaluminium birikmasi asli sifatida tekshirilgan ko-katalizator uchun polimerizatsiya ning alkenlar.[1]
Xususiyatlari
Ko'p alyuminiy organik birikmalar singari, birikmaning tuzilishi, ehtimol, u taklif qilganidan ko'proqdir empirik formula. Turli xil texnikalar, shu jumladan emas Rentgenologik kristallografiya, birikmaning a sifatida mavjudligini taxmin qiling dimer ko'prikni taqsimlaydigan tetraedral alyuminiy markazlaridan tashkil topgan trimer gidrid ligandlar.[2] Gidridlar kichik va alyuminiy hosilalari uchun juda katta Asosiy, shuning uchun ular afzallik sifatida ko'prik alkil guruhlar.
DIBALni isitish orqali tayyorlash mumkin triizobutilaluminium (o'zi dimer) qo'zg'atish uchun beta-gidridni yo'q qilish:[3]
- (men-Bu3Al)2 → (men-Bu2AlH)2 + 2 (CH3)2C = CH2
DIBALni tijorat maqsadlarida rangsiz suyuqlik sifatida sotib olish mumkin bo'lsa-da, u ko'proq sotib olinadi va organik erituvchida eritma sifatida tarqatiladi. toluol yoki geksan.
Organik sintezda foydalaning
DIBAL foydali bo'ladi organik sintez konvertatsiya qilishni o'z ichiga olgan turli xil pasayishlar uchun karbon kislotalari, ularning hosilalari va nitrillar ga aldegidlar. DIBAL a-b to'yinmagan efirlarni mos keladigan allil spirtiga kamaytiradi.[4] Aksincha, LiAlH4 esterlarni kamaytiradi va asil xloridlar birlamchi spirtli ichimliklar va nitrillar birlamchi ominlar [Fieser ish protsedurasidan foydalangan holda]. DIBAL elektronlarga kam birikmalar bilan sekin, elektronlarga boy birikmalar bilan tezroq reaksiyaga kirishadi. Shunday qilib, bu elektrofil kamaytirish agenti, LiAlH esa4 deb o'ylash mumkin nukleofil kamaytiruvchi vosita.
DIBAL ishonchli ravishda nitrillarni aldegidlarga kamaytirsa-da, efirlarni bir xil funktsional guruhga qaytarishi shafqatsiz nozik reaktsiya bo'lib, u qog'ozga foydali ko'rinadi, ammo amalda ko'pincha spirt va aldegid aralashmalariga olib keladi. Ushbu muammo doimiy oqim kimyosi yordamida reaksiya sharoitlarini sinchkovlik bilan boshqarish orqali hal qilindi.[5]
Xavfsizlik
DIBAL, ko'pgina alkilaluminiy birikmalari singari, havo va suv bilan kuchli reaksiyaga kirishib, yong'inlarga olib kelishi mumkin.
Adabiyotlar
- ^ Zigler, K.; Martin, H.; Krupp, F. (1960). "Metallorganische Verbindungen, XXVII Aluminiumtrialkyle und Dialkyl-Aluminiumhydride aus Aluminiumisobutyl-Verbindungen". Yustus Libigs Annalen der Chemie. 629 (1): 14–19. doi:10.1002 / jlac.19606290103.
- ^ Self, M. F .; Pennington, V. T.; Robinson, G. H. (1990). "Diizobutilaluminiy gidridning makrosiklik tetradentat ikkilamchi amin bilan reaksiyasi. [Al (iso-Bu)] ning sintezi va molekulyar tuzilishi2[C10H20N4] [Al (iso-Bu)3]2: (Iso-Bu) ning g'ayritabiiy mutanosibligi dalili2AlH ". Inorganica Chimica Acta. 175 (2): 151–153. doi:10.1016 / S0020-1693 (00) 84819-7.
- ^ Eisch, J. J. (1981). Organometalik sintezlar. 2. Nyu-York: Academic Press. ISBN 0-12-234950-4.
- ^ Galatsis, P. (2001). "Diizobutilaluminiy gidrid". Organik sintez uchun reaktivlar entsiklopediyasi. Nyu-York: John Wiley & Sons. doi:10.1002 / 047084289X.rd245. ISBN 0471936235.
- ^ Uebb, Damin; Jamison, Timoti F. (2012-01-20). "Diizobutilaluminium gidridning kamayishi qayta tiklandi: Aldegid sintezi uchun tezkor, mustahkam va tanlangan doimiy oqim tizimi". Organik xatlar. 14 (2): 568–571. doi:10.1021 / ol2031872. hdl:1721.1/76286. ISSN 1523-7060. PMID 22206502.
Tashqi havolalar
- Stockman, R. (2001). "Metil efirdan olingan aminokislotaning diballi kamayishi; Garnerning aldegidi". ChemSpider sintetik sahifalari. doi:10.1039 / SP161. 161-bet.[doimiy o'lik havola ]
- "Organik kimyoda oksidlanish va qaytarilish reaktsiyalari". Janubiy Meyn universiteti, kimyo kafedrasi. Arxivlandi asl nusxasi 2011-06-11.
- "Diisobutil alyuminiy gidrid (DIBAL-H) va boshqa izobutil alyuminiy alkillar (DIBAL-BOT, TIBAL) maxsus organik sintez reaktivlari sifatida" (PDF). Akzo-Nobel. Arxivlandi asl nusxasi (PDF) 2011-04-08 da. Olingan 2011-02-23.
