Enoyl-CoA gidrataza - Enoyl-CoA hydratase
| enoyl-koenzim A, gidrataza / 3-gidroksiatsil koenzim A dehidrogenaza | |||||||
|---|---|---|---|---|---|---|---|
 Sichqonchadan Enoyl-CoA gidrataza geksameri faol joyi to'q sariq va substrat qizil rangda. | |||||||
| Identifikatorlar | |||||||
| Belgilar | EHADH | ||||||
| Alt. belgilar | ECHD | ||||||
| NCBI geni | 1962 | ||||||
| HGNC | 3247 | ||||||
| OMIM | 607037 | ||||||
| RefSeq | NM_001966 | ||||||
| UniProt | Q08426 | ||||||
| Boshqa ma'lumotlar | |||||||
| EC raqami | 4.2.1.17 | ||||||
| Lokus | Chr. 3 q26.3-q28 | ||||||
| |||||||
Enoyl-CoA gidrataza (ECH) yoki krotonaza[1] bu ferment Ikkinchi va uchinchi o'rtasidagi er-xotin bog'lanishni namlaydi uglerodlar 2-trans / cis-enoyl-CoA da:[2]

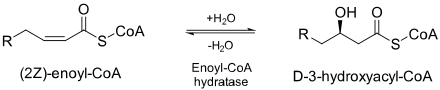
ECH juda muhimdir metabolizm yog 'kislotalari yilda beta oksidlanish ikkalasini ham ishlab chiqarish atsetil CoA va energiya shaklida ATP.[2]
Kalamushlarning ECH - bu a geksamerik oqsil (bu xususiyat universal emas, lekin odam fermenti ham heksamerikdir), bu esa ushbu fermentning samaradorligiga olib keladi, chunki u 6 ta faol saytga ega. Ushbu ferment juda samarali ekanligi aniqlandi va odamlarga yog 'kislotalarini juda tez energiyaga aylantirishga imkon beradi. Aslida bu ferment shu qadar ta'sirchanki, stavka chunki qisqa zanjirli yog 'kislotalari diffuziya bilan boshqariladigan oksidga tengdir reaktsiyalar.[3]
Metabolizm
Yog 'kislotasi metabolizmi
ECH kataliz qiladi yog 'kislotalarining parchalanishidagi ikkinchi bosqich (gidratatsiya)b-oksidlanish ).[4] Yog 'kislotasi almashinuvi - bu inson tanasi qanday aylanadi yog'lar energiyaga. Oziq-ovqatlardagi yog'lar odatda shaklida bo'ladi triglitserollar. Yog'lar inson tanasiga o'tishi uchun bularni parchalash kerak. Bu sodir bo'lganda, uchta yog 'kislotasi ajralib chiqadi.
Leytsin metabolizmi
Mexanizm
ECH gidroksil guruhini va a qo'shish uchun b-oksidlanishda ishlatiladi proton to'yinmaganlarga b-uglerod yog'li-asil CoA ustida. ECH ikkitasini ta'minlash orqali ishlaydi glutamat qoldiqlar katalitik sifatida kislota va tayanch. Ikki aminokislotalar ushlab turing suv molekula o'rnida, unga hujum qilishga imkon beradi sin qo'shilishi b-uglerodda a-b to'yinmagan asil-CoA ga. Keyin a-uglerod yana bir protonni ushlaydi, bu esa beta-gidroksi asil-KoA hosil bo'lishini yakunlaydi.

Protonlarning boshqa biron bir manbasi mavjud emasligi eksperimental ma'lumotlardan ma'lum faol sayt. Bu shuni anglatadiki, a-uglerod tutadigan proton b-uglerodga hujum qilgan suvdan. Buning ma'nosi shundan iboratki, gidroksil guruhi va suvdan proton ikkala tomonning bir tomonidan qo'shiladi qo'shaloq bog'lanish, sin qo'shimchasi. Bu ECHga S hosil qilishga imkon beradi stereoizomer 2-trans-enoyl-CoA dan va 2-cis-enoyl-CoA dan R stereoizomer. Bu ikkalasi tomonidan amalga oshiriladi glutamat suvni a-b to'yinmagan er-xotin bog'lanishiga bevosita tutash holatda ushlab turadigan qoldiqlar. Ushbu konfiguratsiya ECH uchun faol joyni juda qattiq bo'lishini talab qiladi, bu suvni asil-KoA ga nisbatan juda aniq konfiguratsiyaga ega bo'lishi kerak. A uchun ma'lumotlar mexanizm chunki bu reaktsiya bu reaktsiyaning kelishilganligi (rasmda ko'rsatilgan) yoki ketma-ket bosqichlarda sodir bo'ladimi degan xulosaga kelmaydi. Agar ketma-ket qadamlar bilan sodir bo'ladigan bo'lsa, qidiruv an hosil bo'ladigan bilan bir xil bo'ladi E1cB-yo'q qilish reaktsiyasi.[8]
ECH mexanik jihatdan o'xshashdir fumaraza.
Adabiyotlar
- ^ "EC 4.2.1.17". www.sbcs.qmul.ac.uk. Olingan 2018-09-05.
- ^ a b Allenbax, L; Poirier, Y (2000). "Transoksik o'simliklardan foydalangan holda to'yinmagan yog'li kislotalarning b-oksidlanishining muqobil yo'llarini tahlil qilish Peroxisomalarda polihidroksialankanatlarni sintez qilish". O'simliklar fiziologiyasi. 124 (3): 1159–1168. doi:10.1104 / s.124.3.1159. ISSN 0032-0889. PMC 59215. PMID 11080293.
- ^ Engel CK, Kiema TR, Xiltunen JK, Vierenga RK (fevral, 1998). "Oktanoil-KoA bilan komplekslangan enoyl-KoA gidratazaning kristalli tuzilishi uzoq zanjirli yog 'kislotasi-CoA molekulasini bog'lash uchun zarur bo'lgan tuzilish moslamalarini ochib beradi". Molekulyar biologiya jurnali. 275 (5): 847–59. doi:10.1006 / jmbi.1997.1491. PMID 9480773.
- ^ Cox DL, Nelson MM (2005). Biokimyoning lehninger tamoyillari (4-nashr). Nyu-York: W.H. Freeman. p.647-43. ISBN 978-0-7167-4339-2.
- ^ a b Wilson JM, Fitschen PJ, Kempbell B, Uilson GJ, Zanchi N, Teylor L, Uilborn C, Kalman DS, Stout JR, Hoffman JR, Ziegenfuss TN, Lopez HL, Kreider RB, Smit-Rayan AE, Antonio J (fevral 2013) . "Xalqaro sport ovqatlanish pozitsiyasi stendi: beta-gidroksi-beta-metilbutirat (HMB)". Xalqaro sport oziqlanish jamiyati jurnali. 10 (1): 6. doi:10.1186/1550-2783-10-6. PMC 3568064. PMID 23374455.
- ^ a b Kolmeyer M (may, 2015). "Leytsin". Oziq moddalar almashinuvi: tuzilmalar, funktsiyalar va genlar (2-nashr). Akademik matbuot. 385-388 betlar. ISBN 978-0-12-387784-0. Olingan 6 iyun 2016.
Energiya yoqilg'isi: Oxir oqibat Leu ko'pi parchalanib, taxminan 6,0kkal / g ni tashkil qiladi. Yutilgan Leuning taxminan 60% bir necha soat ichida oksidlanadi ... Ketogenez: muhim qismi (yutilgan dozaning 40%) atsetil-KoA ga aylanadi va shu bilan ketonlar, steroidlar, yog 'kislotalari va boshqalarning sinteziga hissa qo'shadi. birikmalar
Shakl 8.57: ning metabolizmi L-leytsin - ^ Bahnson BJ, Anderson VE, Petsko GA (2002 yil fevral). "Enoyl-CoA gidratazaning tuzilish mexanizmi: bitta suvdan uchta atom E1cb bosqichma-bosqich yoki kelishilgan holda qo'shiladi". Biokimyo. 41 (8): 2621–9. doi:10.1021 / bi015844p. PMID 11851409.
Tashqi havolalar
- Enoyl-KoA + Gidrataza AQSh Milliy tibbiyot kutubxonasida Tibbiy mavzu sarlavhalari (MeSH)

