Nitratsiya - Nitration
Yilda organik kimyo, nitratlash ning umumiy sinfi kimyoviy jarayonlar nitro kiritilishi uchun guruh ichiga organik birikma. Ushbu atama nitrat hosil qilishning turli jarayonlariga noto'g'ri qo'llaniladi Esterlar o'rtasida spirtli ichimliklar va azot kislotasi (sodir bo'lganidek sintez ning nitrogliserin ). Olingan natijalar orasidagi farq molekulyar tuzilmalari nitro birikmalari va nitratlar bu azot nitro birikmalaridagi atom to'g'ridan-to'g'ri bog'langan boshqalargakislorod atom (odatda uglerod yoki boshqa azot atomi), nitrat efirlarida (organik nitratlar deb ham ataladi) azot kislorod atomi bilan bog'langan bo'lib, u odatda uglerod atomi (nitrito guruhi) bilan bog'lanadi.
Qattiq ma'noda nitratlashning ko'plab yirik sanoat dasturlari mavjud; kabi nitroaromatik birikmalar ishlab chiqarish uchun hajmi bo'yicha eng muhimi nitrobenzol. Nitratsiya reaktsiyalari, ayniqsa, portlovchi moddalarni ishlab chiqarish uchun ishlatiladi, masalan konvertatsiya qilish guanidin ga nitroguanidin va konvertatsiya qilish toluol ga trinitrotoluol (TNT). Biroq, ular juda katta ahamiyatga ega kimyoviy vositalar va kashshoflar. Yiliga millionlab tonna nitroaromatika ishlab chiqariladi.[1]
Aromatik nitratsiya
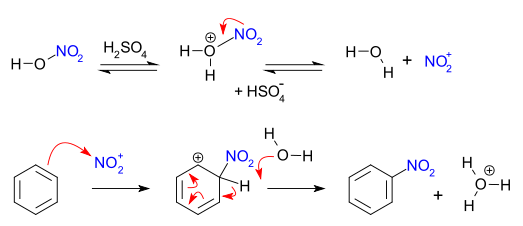
Oddiy nitratsiya sintezlari "aralash kislota" deb ataladigan, konsentrlangan aralashmani qo'llaydi azot kislotasi va sulfat kislotalar.[2] Ushbu aralashma hosil qiladi nitron ioni (YO'Q2+), bu faol turlar aromatik nitratsiya. Bu holda ajratilishi mumkin bo'lgan ushbu faol moddalar nitroniy tetrafloroborat,[3] shuningdek aralash nitratga ehtiyoj sezmasdan nitratsiyani ta'sir qiladi. Aralash kislota sintezlarida oltingugurt kislotasi iste'mol qilinmaydi va shuning uchun a katalizator shuningdek, suv uchun changni yutish vositasi. Nitratlangan taqdirda benzol, reaksiya iliq haroratda, 50 ° C dan yuqori bo'lmagan holda o'tkaziladi. [4] Jarayon bunga misoldir elektrofil aromatik almashtirish, bu elektronlarga boy hujumni o'z ichiga oladi benzol uzuk:
Shu bilan bir qatorda alternativ mexanizmlar, jumladan bitta elektron uzatishni o'z ichiga olgan mexanizm (SET) taklif qilingan.[5][6]
Qo'llash sohasi
Nitratsiyalarda selektivlik qiyin bo'lishi mumkin, chunki qoida tariqasida bir nechta birikmalar paydo bo'lishi mumkin, ammo ulardan bittasi kerak bo'ladi, shuning uchun muqobil mahsulotlar ifloslantiruvchi rol o'ynaydi yoki shunchaki isrof qilinadi. Shunga ko'ra, sintezlarni tegishli selektiv bilan loyihalash maqsadga muvofiqdir; masalan, reaktsiya sharoitlarini boshqarish orqali, ftorenon tanlab trinitratsiya qilish mumkin[7] yoki tetranitratlangan.[8]
Xushbo'y halqalardagi o'rnini bosuvchi moddalar stavka bu elektrofil aromatik almashtirish. Guruhlarni o'chirish boshqalar kabi nitro guruhlar elektronni tortib olish effektiga ega. Bunday guruhlar reaktsiyani o'chiradi (sekinlashtiradi) va elektrofil nitronium ionini hujumga yo'naltiradi aromatik meta holati. O'chirish meta-yo'naltiruvchi o'rinbosarlar kiradi sulfanil, siyano guruhlar, keto, Esterlar va karboksilatlar. Nitratsiyani tezlashtirish mumkin guruhlarni faollashtirish kabi amino, gidroksi va metil guruhlar ham amidlar va efirlar natijada para va orto izomerlari paydo bo'ladi.
Ning to'g'ridan-to'g'ri nitratsiyasi anilin bilan azot kislotasi va sulfat kislota, bitta manbaga ko'ra,[9] natijasida 50/50 aralashmasi hosil bo'ladi paragraf- va meta-nitroanilin izomerlari. Ushbu reaktsiyada tez reaksiyaga kirishuvchi va faollashtiruvchi anilin (ArNH)2) aniliniyum ioni (ArNH) ko'proq, ammo unchalik reaktiv bo'lmagan (o'chirilgan) muvozanatda mavjud3+), bu reaktsiya mahsulotining tarqalishini tushuntirishi mumkin. Boshqa manbaga ko'ra,[10] anilinni ko'proq boshqariladigan nitratsiyasi hosil bo'lishidan boshlanadi asetanilid bilan reaksiya orqali sirka angidrid undan keyin haqiqiy nitratsiya. Amid muntazam faollashtiruvchi guruh bo'lganligi sababli hosil bo'lgan mahsulotlar para va orto izomerlari hisoblanadi. Reaktsiya aralashmasini qizdirish amidni yana nitratlangan anilinga gidroliz qilish uchun etarli.
In Volfenshteyn - Boteers reaktsiyasi, benzol nitrat kislota bilan reaksiyaga kirishadi va simob (II) nitrat bermoq prikol kislotasi.
Ipso nitratsiyasi
Aril xloridlar bilan, triflates va nonflatlar ipso almashtirish deb nomlangan joyda ham bo'lishi mumkin ipso nitratsiyasi.[11] Ushbu iborani Perrin va Skinner birinchi marta 1971 yilda xloroanizol nitratsiyasini tekshirishda qo'llashgan [12] Bitta protokolda 4-xlor-n-butilbenzol bilan reaksiyaga kirishadi natriy nitrit yilda t-butanol 0,5 mol% ishtirokida Pd2(dba)3, biarilfosfin ligand va a fazali uzatish katalizatori 4-nitro- ga qadarn-butilbenzol.[13]
Shuningdek qarang
Adabiyotlar
- ^ Jerald But (2007). "Nitro aralashmalari, aromatik". Ullmannning Sanoat kimyosi ensiklopediyasi. Vaynxaym: Vili-VCH. doi:10.1002 / 14356007.a17_411.
- ^ John McMurry Organik kimyo 2-chi nashr.
- ^ Jorj A. Olax va Stiven J. Kun. "Benzonitril, 2-metil-3,5-dinitro-". Organik sintezlar.; Jamoa hajmi, 5, p. 480
- ^ https://www.chemguide.co.uk/organicprops/arenes/nitration.html
- ^ Esteves, P. M.; Karneiro, J. W. M.; Kardoso, S. P .; Barbosa, A. G. H.; Laali, K. K .; Rasul, G.; Prakash, G. K. S .; e Olah, G. A. (2003). "Elektrofil aromatik nitratning yagona mexanizmi kontseptsiyasi qayta ko'rib chiqildi: hisoblash natijalari va eksperimental ma'lumotlarning yaqinlashuvi". J. Am. Kimyoviy. Soc. 125 (16): 4836–49. doi:10.1021 / ja021307w. PMID 12696903.
- ^ Keyrush, J. F .; Karneiro, J. W. M.; Sabino A. A .; Sparapan, R .; Eberlin, M. N .; Esteves, P. M. (2006). "Elektrofil aromatik nitratsiya: uning mexanizmi va o'rnini bosuvchi ta'sirini tushunish". J. Org. Kimyoviy. 71 (16): 6192–203. doi:10.1021 / jo0609475. PMID 16872205.
- ^ E. O. Vulfolk va Milton Orchin. "2,4,7-Trinitrofloronon". Organik sintezlar.; Jamoa hajmi, 3, p. 837
- ^ Melvin S. Nyuman va H. Boden. "2,4,5,7-Tetranitrofloronon". Organik sintezlar.; Jamoa hajmi, 5, p. 1029
- ^ Veb-resurs: warren-wilson.edu
- ^ Mexanizm va sintez Piter Teylor, Qirollik kimyo jamiyati (Buyuk Britaniya), Ochiq universitet
- ^ Prakash, G.; Metyu, T. (2010). "Arenalarning ipso-nitratsiyasi". Angewandte Chemie International Edition ingliz tilida. 49 (10): 1726–1728. doi:10.1002 / anie.200906940. PMID 20146295.
- ^ Perrin, K. L .; Skinner, G. A. (1971). "Elektrofil aromatik almashtirishdagi direktiv effektlar (" ipso omillar "). Galoanizollarni nitratsiyasi". Amerika Kimyo Jamiyati jurnali. 93 (14): 3389. doi:10.1021 / ja00743a015.
- ^ Fors, B .; Buchvald, S. (2009). "Pry-katalizlangan aril xloridlar, triflatlar va nonaflatlarning nitroaromatikaga aylanishi". doi:10.1021 / ja905768k. PMC 2773681. PMID 19737014. Iqtibos jurnali talab qiladi
| jurnal =(Yordam bering)