Bioavailability - Bioavailability - Wikipedia
Yilda farmakologiya, bioavailability (BA yoki F) ning pastki toifasi singdirish va boshqariladigan qism (%) dori ga etib boradi tizimli aylanish.[1]
Ta'rifga ko'ra, dori qo'llanilganda vena ichiga, uning bioavailability 100% ni tashkil qiladi.[2][3] Ammo, dori orqali yuborilganda marshrutlar vena ichiga yuborishdan tashqari, uning bioavailability odatda[TH] ichak endoteliyasining singishi tufayli tomir ichiga yuborilganidan past va birinchi o'tish metabolizmi. Shunday qilib, matematik jihatdan, bioavailability solishtirish nisbati bilan tenglashadi plazmadagi konsentratsiya egri chizig'i ostidagi maydon vaqtga nisbatan (AUC) tomir ichidagi formulasi uchun AUC ga ekstravaskulyar formulasi uchun.[4] AUC dan foydalaniladi, chunki AUC tizimli qon aylanishiga tushgan dozaga mutanosibdir.[5]
Preparatning bioavailability an o'rtacha qiymat; olmoq aholi o'zgaruvchanligi hisobga olish, og'ish oralig'i sifatida ko'rsatilgan ±.[4] Yomon emilimiga ega bo'lgan giyohvand moddalarni iste'mol qiluvchining dozasini mos ravishda berishini ta'minlash uchun, og'ish oralig'ining pastki qiymati haqiqiy bioavailabilityni ifodalash va tomir ichiga yuborish kabi tizimli konsentrasiyalarga erishish uchun dori qabul qiluvchiga zarur bo'lgan dori dozasini hisoblash uchun ishlatiladi.[4] Preparatni qabul qiluvchining so'rilish tezligini bilmagan holda dozalash uchun, agar preparat tor bilan bog'liq bo'lmasa, mo'ljallangan samaradorlikni ta'minlash uchun og'ish oralig'ining pastki qiymati qo'llaniladi. terapevtik oyna.[4]
Uchun xun takviyeleri Qo'llash usuli deyarli har doim og'iz orqali bo'lgan o'tlar va boshqa oziq moddalar, bioavailability odatda so'rilgan dozaning miqdori yoki qismini belgilaydi.[6][7][8]
Ta'riflar
Farmakologiyada
Farmakologiyada bioavailability - bu dori ta'sir joyiga etib borishi tezligi va darajasi.[9]Bu harf bilan belgilanadi f (yoki foizda ifodalangan bo'lsa, tomonidan F).
Oziqlantirish fanlarida
Oziq moddalar va giyohvand bo'lmagan parhez tarkibiy qismlarini iste'mol qilishni o'z ichiga olgan ovqatlanish fanlarida bioavailability tushunchasi farmatsevtika sanoati bilan bog'liq aniq belgilangan standartlarga ega emas. Farmakologik ta'rif ushbu moddalarga taalluqli emas, chunki utilizatsiya va emilim sub'ektning ozuqaviy holati va fiziologik holatining vazifasidir,[10] natijada individualdan individualgacha (individuallararo o'zgaruvchanlik) yanada katta farqlar paydo bo'ladi. Shuning uchun, xun takviyeleri uchun bioavailability, so'rilishi mumkin bo'lgan va foydalanish yoki saqlash uchun mavjud bo'lgan moddaning ulushi sifatida aniqlanishi mumkin.[11]
Ikkalasida ham farmakologiya va ovqatlanish fanlari, bioavailability hisoblash yo'li bilan o'lchanadi egri chiziqli maydon Preparat konsentratsiyasi vaqt rejimining (AUC).
Atrof-muhit fanlari yoki fanlar bo'yicha
Bioavailability bu atrof-muhitdagi turli xil moddalarning tirik organizmlarga kirib borishi o'lchovidir. Odatda bu ekinlarni etishtirishda (eruvchanligini cheklashi yoki o'simliklarning ozuqaviy elementlarini tuproq kolloidlariga singishi sababli) va oziq-ovqat zanjiridan toksik moddalarni mikroorganizmlar tomonidan olib tashlashda (boshqa yo'l bilan parchalanadigan moddalarga singishi yoki bo'linishi sababli) cheklovchi omil hisoblanadi. atrof-muhitdagi erishib bo'lmaydigan fazalar). Qishloq xo'jaligi uchun e'tiborga loyiq misol - temir va alyuminiy fosfatlar bilan yog'ingarchilik natijasida o'simlik fosforining etishmasligi tuproq pH qiymati va yuqori tuproq pH darajasida kaltsiy fosfatlar bilan yog'ingarchilik.[12] Tuproqdagi zaharli materiallar, masalan, bo'yoqdan qo'rg'oshin, fosforli o'g'itlarni ortiqcha miqdorda etkazib berish orqali ifloslangan tuproqni yutadigan hayvonlar uchun yaroqsiz holga kelishi mumkin.[13] Organik ifloslantiruvchi moddalar, masalan, erituvchi yoki pestitsidlar[14] mikroorganizmlar uchun yaroqsiz bo'lib qolishi mumkin va shuning uchun ular tuproq minerallariga singib ketganda atrof muhitda saqlanib qoladi[15] yoki hidrofobik organik moddalarga bo'linish.[16]
Mutlaq bioavailability
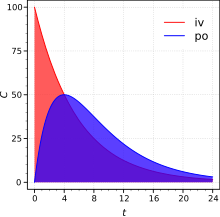
Mutlaq bioavailability faol preparatning tizimli qon aylanishida biologik mavjudligini taqqoslaydivena ichiga yuborish ma'muriyat (ya'ni, keyin og'zaki, bukkal, okulyar, burun, rektal, transdermal, teri osti, yoki til osti vena ichiga yuborilgandan keyin bir xil preparatning bioavailability bilan. Bu preparatning vena ichiga yuborish bilan taqqoslaganda, vena ichiga yuborilmasdan so'rilgan dori qismidir. Taqqoslash dozani normallashtirishi kerak (masalan, turli dozalarni yoki sub'ektlarning turli og'irliklarini hisobga olish); Binobarin, so'rilgan miqdor, kiritilgan dozani taqsimlash yo'li bilan tuzatiladi.
Farmakologiyada preparatning mutlaq bioavailabilityligini aniqlash uchun, a farmakokinetik a olish uchun o'rganish kerak plazmadagi dori konsentratsiyasi va vaqt Vena ichiga (iv) va ekstravaskulyar (vena ichiga yuborilmasdan, ya'ni og'iz orqali) yuborilgandan keyin preparat uchun fitna. Mutlaq bioavailability bu egri chiziq ostida dozani to'g'irlaydigan maydon (AUC) vena ichiga yuborilmagan AUC vena ichiga yuborish. Mutlaq bioavailabilityni hisoblash formulasi, F, og'iz orqali yuborilgan preparatning (po) quyida keltirilgan (qaerda D. doza kiritiladi).
Shuning uchun tomir orqali yuboriladigan preparat mutlaqo 100% bioavailabilityga ega bo'ladi (f = 1), boshqa yo'llar bilan berilgan dorilar odatda mutlaq bioavailabilityga ega Kamroq Agar bir xil faol moddalarga ega bo'lgan ikki xil dozalash shakllarini taqqoslasak va ikkita dori vositasining biologik mavjudligini taqqoslasak, qiyosiy bioavailability deyiladi.[iqtibos kerak ]
Tizimli emilimning haqiqiy darajasini bilish (mutlaq bioavailability deb ataladi) aniq foydali bo'lsa-da, amalda u o'ylagandek tez-tez aniqlanmaydi. Buning sababi shundaki, uni baholash talab qilinadi vena ichiga yuborish; ya'ni barcha kiritilgan dori-darmonlarni kafolatlaydigan qabul qilish usuli tizimli qon aylanishiga etadi. Bunday tadqiqotlar katta xarajatlarga olib keladi, shularning kamida bittasi xavfsizlikni ta'minlash uchun klinikadan oldin toksiklik sinovlarini o'tkazish zarurati, shuningdek, eruvchanlik cheklovlari sababli yuzaga kelishi mumkin bo'lgan muammolardir. Ammo ushbu cheklovlarni anning juda past dozasini (odatda bir necha mikrogram) yuborish orqali engib o'tish mumkin izotopik etiketli dori terapevtik izotopik bo'lmagan etiketli og'iz dozasi bilan bir vaqtda (izotopik tarzda belgilangan tomir ichiga yuboriladigan doz, etiketlanmagan og'iz dozasidan erishilgan tizimli dori konsentratsiyasini buzmaslik uchun etarli darajada past). Keyinchalik tomir ichiga va og'iz orqali kontsentratsiyani turli xil izotopik konstitutsiyasi tufayli dekonvolutatsiya qilish mumkin va shu bilan og'iz orqali yuborish va tomir ichiga yuborish farmakokinetikasini bir xil dozadan foydalanish mumkin. Ushbu uslub ekvivalent bo'lmagan klirens bilan farmakokinetik muammolarni bartaraf qiladi, shuningdek tomir ichiga yuboriladigan dozani minimal toksikologiya va formulalar bilan kiritishga imkon beradi. Texnik birinchi navbatda barqaror-izotoplar yordamida qo'llanilgan 13Izotoplarni massa farqi bilan ajratish uchun C va mass-spektrometriya. Yaqinda, 14C markali preparatlar vena ichiga yuboriladi va izotopik etiketli preparatni o'lchash uchun ishlatiladigan tezlashtiruvchi mass-spektrometriya (AMS) va etiketasiz dori uchun mass-spektrometriya.[17]
Vena ichiga yuboriladigan farmakokinetikani yoki mutlaq bioavailabilityni belgilash uchun me'yoriy talablar mavjud emas, ammo tartibga solish organlari ba'zan bioavailability ko'rinadigan darajada past yoki o'zgaruvchan bo'lgan holatlarda va ekstravaskulyar yo'lning mutlaq bioavailability ma'lumotlarini so'rashadi. farmakodinamikasi va terapevtik dozalarda farmakokinetikasi. Bunday holatlarda mutlaq bioavailability tadqiqotini o'tkazish uchun preparatni vena ichiga yuborish kerak.[18]
Rivojlantiruvchi preparatni vena ichiga yuborish. Ning asosiy farmakokinetik parametrlari to'g'risida qimmatli ma'lumot berishi mumkin tarqatish hajmi (V) va tozalash (CL).[18]
Nisbiy bioavailability va bioekvivalensiya
Farmakologiyada nisbiy bioavailability bioavailabilityni o'lchaydi (deb taxmin qilinadi AUC) bir xil preparatning boshqa formulasi (B) bilan taqqoslaganda ma'lum bir preparatning (A) formulasi, odatda belgilangan standart yoki boshqa yo'l bilan yuborish orqali. Agar standart tomir ichiga yuboriladigan preparatdan iborat bo'lsa, bu mutlaq bioavailability deb nomlanadi (qarang yuqorida ).
Nisbiy bioavailability - bu baholash uchun ishlatiladigan choralardan biridir bioekvivalentlik (BO'LING) ikki dori vositasi o'rtasida. FDA tomonidan tasdiqlanish uchun umumiy ishlab chiqaruvchi 90% ko'rsatishi kerak ishonch oralig'i o'rtacha javoblarning nisbati uchun (odatda AUC va maksimal konsentratsiya, Cmaksimal) mahsulotini "tovar nomi bilan"[OB] 80% dan 125% gacha. Qaerda AUC vaqt o'tishi bilan qonda preparatning konsentratsiyasini anglatadi t = 0 dan t = ∞, Cmaksimal preparatning qondagi maksimal kontsentratsiyasini anglatadi. Qachon Tmaksimal berilgan, bu preparat yetib borishi uchun zarur bo'lgan vaqtni anglatadi Cmaksimal.
Formulaning bioavailability va bioekvivalensiyaga ta'sir qilish mexanizmlari dorilarda keng o'rganilgan bo'lsa-da, ozuqaviy qo'shimchalardagi bioavailability va bioequivalentsiyaga ta'sir qiluvchi formulyatsion omillar asosan noma'lum.[19] Natijada, ozuqaviy fanlarda nisbiy bioavailability yoki bioequivalence bioavailabilityning eng keng tarqalgan o'lchovidir, bir xil parhez tarkibiy qismining bir formulasining bioavailability bilan boshqasini taqqoslaydi.
Bioavailabilityga ta'sir qiluvchi omillar
Ekstravaskulyar yo'l bilan yuborilganda preparatning mutlaq bioavailability odatda bitta (ya'ni, F<100%). Turli xil fiziologik omillar dori vositalarining tizimli qon aylanishiga kirishidan oldin ularni kamaytiradi. Preparat oziq-ovqat bilan yoki qo'shilmasdan qabul qilinishidan qat'i nazar, so'rilish jarayoniga ta'sir qilishi mumkin, boshqa qabul qilingan preparatlar so'rilishini va birinchi o'tish metabolizmini o'zgartirishi mumkin, ichak harakatlanishi preparatning tarqalishini o'zgartiradi va preparatning ichak mikroflorasi bilan kimyoviy parchalanish darajasiga ta'sir qilishi mumkin. Jigar metabolizmi yoki oshqozon-ichak traktining ta'siriga ta'sir qiluvchi kasallik holatlari ham ta'sir qiladi.
Boshqa omillar quyidagilarni o'z ichiga olishi mumkin, lekin ular bilan chegaralanmaydi:
- Preparatning fizik xususiyatlari (hidrofobiklik, pKa, eruvchanlik )
- Preparatni shakllantirish (zudlik bilan chiqarish, ishlatiladigan yordamchi moddalar, ishlab chiqarish usullari, o'zgartirilgan versiya - kechiktirilgan chiqish, uzaytirilgan muddat, uzoq muddatli ozod qilish va hk)
- Formulyatsiya oziqlanadigan yoki boshqariladimi ro'za tutdi davlat
- Oshqozonni bo'shatish darajasi
- Sirkadiyalik farqlar
- Boshqa dorilar / ovqatlar bilan o'zaro ta'siri:
- Boshqa dorilar bilan ta'sir o'tkazish (masalan, antatsidlar, alkogol, nikotin)
- Boshqa ovqatlar bilan o'zaro aloqalar (masalan, greyfurt sharbati, pomello, kızılcık suvi, brassika sabzavotlar
- Tashuvchilar: substrat oqish transportchilar (masalan.) P-glikoprotein )
- Salomatligi oshqozon-ichak trakti
- Ferment boshqa dorilar / ovqatlar tomonidan indüksiyon / inhibisyon:
- Metabolik farqlarning individual o'zgarishi
- Yoshi: Umuman olganda, dorilar homila, neonatal va geriatrik populyatsiyalarda sekinroq metabollanadi
- Fenotipik farqlar, enterohepatik qon aylanishi, parhez, jins
- Kasallik holati
Ushbu omillarning har biri har bir bemorda o'zgarishi mumkin (individual o'zgaruvchanlik) va haqiqatan ham bir bemorda vaqt o'tishi bilan (individual individual o'zgarish). Yilda klinik sinovlar, individual individual variatsiya - bu taxmin qilinadigan dozalashni ta'minlash uchun bemordan bemorga bioavailability farqlarini baholash uchun ishlatiladigan muhim o'lchov.
Dori-darmonlarga nisbatan biologik mavjudlik
Giyohvand moddalar bilan taqqoslaganda, ularning biologik mavjudligini baholashga ta'sir ko'rsatadigan xun takviyalarida sezilarli farqlar mavjud. Ushbu farqlar quyidagilarni o'z ichiga oladi: ozuqaviy qo'shimchalar o'zgaruvchan va ko'pincha sifat jihatidan foyda keltirishi; ozuqa moddalarining emishini o'lchashda aniqlik yo'q; oldini olish va farovonlik uchun ozuqaviy qo'shimchalar iste'mol qilinadi; ozuqaviy qo'shimchalar xarakterli emas doza-javob egri chiziqlari; va ozuqaviy qo'shimchalarning dozalari oralig'i, shuning uchun dori terapiyasidan farqli o'laroq muhim emas.[11]
Bundan tashqari, xun takviyasini iste'mol qilish bo'yicha aniqlangan metodologiya va qoidalarning etishmasligi, dori vositalariga nisbatan bioavailability choralarini qo'llashga to'sqinlik qiladi. Oziq-ovqat qo'shimchalari bilan o'tkazilgan klinik sinovlarda bioavailability birinchi navbatda davolash guruhlari o'rtasidagi o'rtacha yoki o'rtacha AUC farqlarining statistik tavsiflariga e'tibor beradi, shu bilan birga ularning standart og'ishlarini yoki individual o'zgarishini solishtirib yoki muhokama qila olmaydi. Ushbu muvaffaqiyatsizlik, guruhdagi biron bir odam o'rtacha farqni taqqoslash bilan tavsiflangan afzalliklarga ega bo'ladimi yoki yo'qmi degan savolni ochiq qoldiradi. Bundan tashqari, agar bu masala muhokama qilingan bo'lsa ham, ushbu mavzulararo farqlarning ma'nosini iste'molchilar va / yoki ularning shifokorlariga etkazish qiyin bo'lar edi.
Oziqlantirish fanlari: ishonchli va universal bioavailability
Ushbu muammoni hal qilishning usullaridan biri bu "ishonchli bioavailability" ni sinovdan o'tganlarning 84% va "universal bioavailability" ni o'z ichiga olgan ijobiy bioavailability natijalari (assimilyatsiya oldindan belgilangan mezonga javob beradi) deb aniqlashdir. Ushbu ishonchli universal tizim shifokorlar va iste'molchilar bilan aloqalarni yaxshilaydi, masalan, mahsulot yorliqlariga kiritilgan bo'lsa, ular uchun to'g'ridan-to'g'ri formulaning foydalari to'g'risida ma'lumotli tanlov qilish. Bundan tashqari, ishonchli-universal ramka ishonchlilik oralig'ini yaratishga o'xshaydi, uni statistikistlar uzoq vaqtdan beri kichik namunalar, statistik taxminlarni buzish yoki katta og'ishlar bilan ishlash uchun potentsial echim sifatida taklif qilishgan.[20]
Shuningdek qarang
Izohlar
^ TH: Preparat ko'rsatadigan bir nechta istisnolardan biri F 100% dan ortig'i teofillin. Agar og'iz orqali yuborilsa F 111% ni tashkil qiladi, chunki preparat butunlay so'riladi va tomir ichiga yuborilgandan so'ng o'pkada birinchi o'tish metabolizmi chetlab o'tiladi.[21]
^ OB: Ma'lumotnomada keltirilgan dori vositalari (ya'ni, innovatorlar) va shuningdek, asosida tasdiqlangan umumiy dori vositalari Qisqartirilgan yangi giyohvandlik dasturi FDA-larda berilgan To'q rangli kitob.
Adabiyotlar
- ^ Hebert, Meri F. (2013). "Homiladorlikning onaning dori vositalarining farmakokinetikasiga ta'siri". Homiladorlik paytida klinik farmakologiya. Elsevier. 17-39 betlar. doi:10.1016 / b978-0-12-386007-1.00003-9. ISBN 978-0-12-386007-1.
- ^ Griffin, J. P. Farmatsevtika tibbiyoti darsligi (6-nashr). Jersi: BMJ kitoblari. ISBN 978-1-4051-8035-1.[sahifa kerak ]
- ^ Flinn, Edvard (2007). "Farmakokinetik parametrlar". xPharm: keng qamrovli farmakologiya bo'yicha ma'lumot. Elsevier. 1-3 betlar. doi:10.1016 / b978-008055232-3.60034-0. ISBN 978-0-08-055232-3.
- ^ a b v d Devis, Jennifer L. (2018). "Farmakologik tamoyillar". Ot ichki kasalliklari. Elsevier. 79-137 betlar. doi:10.1016 / b978-0-323-44329-6.00002-4. ISBN 978-0-323-44329-6.
- ^ Johanson, G. (2010). "Dispozitsiyani modellashtirish". Keng qamrovli toksikologiya. Elsevier. 153-177 betlar. doi:10.1016 / b978-0-08-046884-6.00108-1. ISBN 978-0-08-046884-6.
- ^ Xeni, Robert P. (2001). "Biologik mavjudlikni o'lchashga ta'sir qiluvchi omillar, kaltsiyni namuna sifatida qabul qilish". Oziqlanish jurnali. 131 (4): 1344S-8S. doi:10.1093 / jn / 131.4.1344S. PMID 11285351.
- ^ SANDSTEAD, XAROLD X.; AU, WILLIAM (2007). "Sink ** Doktor Karl-Gustaf Elinder Metalllarning toksikologiyasi bo'yicha qo'llanmaning 2-nashrida ushbu bobning muallifi bo'lgan; uning matni ko'rsatma bergan.". Metalllarning toksikologiyasi bo'yicha qo'llanma. Elsevier. 925-947 betlar. doi:10.1016 / b978-012369413-3 / 50102-6. ISBN 978-0-12-369413-3.
Bioavailability parhez talablariga ta'sir qiluvchi asosiy omildir (Sandstrom, 1997). Go'shtli ovqatlar bioavailabilityni osonlashtiradi, ammo hazm bo'lmaydigan Zn-bog'lovchi ligandlar bioavailabilityni pasaytiradi (Mills, 1985).
- ^ Solomons, N.V. (2003). "ZINC | Fiziologiya". Oziq-ovqat fanlari va ovqatlanish bo'yicha ensiklopediya. Elsevier. 6272-6277 betlar. doi:10.1016 / b0-12-227055-x / 01309-2. ISBN 978-0-12-227055-0.
Bioavailability qat'iy ravishda ozuqa moddalarini qabul qilish va metabolizmdan foydalanishni anglatadi.
- ^ Shargel, L .; Yu, A. B. (1999). Amaliy biofarmatsevtika va farmakokinetikasi (4-nashr). Nyu-York: McGraw-Hill. ISBN 978-0-8385-0278-5.[sahifa kerak ]
- ^ Xeni, Robert P. (2001). "Biologik mavjudlikni o'lchashga ta'sir qiluvchi omillar, kaltsiyni namuna sifatida qabul qilish". Oziqlanish jurnali. 131 (4 ta qo'shimcha): 1344-1348S. doi:10.1093 / jn / 131.4.1344S. PMID 11285351.
- ^ a b Srinivasan, V. Srini (2001). "Oziq moddalarning bioavailability: In vitro namoyish qilishning amaliy yondashuvi multivitaminli-mineralli kombinatsiyalangan mahsulotdagi ozuqa moddalarining mavjudligini namoyish etish". Oziqlanish jurnali. 131 (4 ta qo'shimcha): 1349-1350S. doi:10.1093 / jn / 131.4.1349S. PMID 11285352.
- ^ Xinsinger, Filipp (2001). "Rizosferadagi tuproqning noorganik P-ning bioavailability ildiz ta'siridagi kimyoviy o'zgarishlar ta'sirida. O'simlik va tuproq. 237 (2): 173–195. doi:10.1023 / A: 1013351617532. S2CID 8562338.
- ^ Ma, Qi-Ying; Traina, Samuel J.; Logan, Terri J.; Rayan, Jeyms A. (1993). "Apatit yordamida in situ qo'rg'oshin immobilizatsiyasi". Atrof-muhit fanlari va texnologiyalari. 27 (9): 1803–1810. doi:10.1021 / es00046a007.
- ^ Sims, G.K .; Radosevich, M .; U, X.-T .; Traina, S. J. (1991). "Sorbsiyaning pestitsidlarning biologik mavjudligiga ta'siri". Bettsda V. B. (tahrir). Tabiiy va sintetik materiallarning biologik parchalanishi. London: Springer. 119-137 betlar.
- ^ O'Loughlin, Edvard J.; Traina, Samuel J.; Sims, Jerald K. (2000). "Namunaviy gil minerallarning suvli suspenziyalarida 2-metilpiridin biodegradatsiyasiga sorbsiyaning ta'siri". Atrof-muhit toksikologiyasi va kimyo. 19 (9): 2168–2174. doi:10.1002 / va boshqalar.5620190904.
- ^ Sims, Jerald K .; Cupples, Alison M. (1999). "Tuproqdagi pestitsidlarning degradatsiyasini boshqaruvchi omillar". Zararkunandalarga qarshi kurash. 55 (5): 598–601. doi:10.1002 / (SICI) 1096-9063 (199905) 55: 5 <598 :: AID-PS962> 3.0.CO; 2-N.
- ^ Lappin, Grem; Roulend, Malkolm; Garner, R. Kolin (2006). "Odamlarda dori vositalarining mutlaq bioavailabilityligini aniqlashda izotoplardan foydalanish". Giyohvand moddalar almashinuvi va toksikologiya bo'yicha mutaxassislarning fikri. 2 (3): 419–427. doi:10.1517/17425255.2.3.419. PMID 16863443. S2CID 2383402.
- ^ a b Lappin, Grem; Stivens, Lloyd (2008). "Biomedikal tezlashtiruvchi mass-spektrometriya: Metabolizm va farmakokinetikada so'nggi qo'llanmalar". Giyohvand moddalar almashinuvi va toksikologiya bo'yicha mutaxassislarning fikri. 4 (8): 1021–1033. doi:10.1517/17425255.4.8.1021. PMID 18680438. S2CID 95122610.
- ^ Xag, Stiven V.; Husayn, Ajaz S. (2001). "Formulaning bioavailabilityga ta'siri: seminar muhokamasining qisqacha mazmuni". Oziqlanish jurnali. 131 (4 ta qo'shimcha): 1389-1391S. doi:10.1093 / jn / 131.4.1389S. PMID 11285360.
- ^ Kagan, Doniyor; Madhavi, Doddabele; Bank, Jinni; Lachlan, Kennet (2010). "'Umumjahon "va ishonchli" bioavailability talablari: shifokorning ozuqaviy qo'shimchalarga bo'lgan ishonchini oshirishi mumkin bo'lgan mezon " (PDF). Tabiiy tibbiyot jurnali. 2 (1): 1-5. Arxivlandi asl nusxasi (PDF) 2016-03-13. Olingan 2013-02-06.
- ^ Shuppan, D .; Molz, K. H .; Stayb, A. H.; Rietbrock, N. (1981). "Teofillinning barqaror ajralib chiqadigan aminofilin formulasidan bioavailability (Eufillinni kechiktiruvchi tabletkalar) - bir martalik va ko'p martalik dozadan keyin plazmadagi darajalari". Xalqaro Klinik Farmakologiya, Terapiya va Toksikologiya jurnali. 19 (5): 223–227. PMID 7251238.
Manbalar
- Roulend, Malkolm; Tozer, N. (2010). Klinik farmakokinetikasi va farmakodinamikasi: tushuncha va qo'llanilishi (4 nashr). Filadelfiya, Pensilvaniya: Lippincott Uilyams va Uilkins. ISBN 978-0-7817-5009-7.
- Velling, Piter G.; Tse, Frensis L. S.; Dighe, Shrikant V. (1991). Farmatsevtik bioekvivalentlik. Dori vositalari va farmatsevtika fanlari. 48. Nyu-York, NY: Marsel Dekker. ISBN 978-0-8247-8484-3.
- Xaushke, Diter; Shtaynjans, Volker; Kabutar, Iris (2007). "Bir va ko'p dozali bioekvivalentlikni o'rganishdagi konsentratsiyali vaqt rejimlarini tavsiflovchi ko'rsatkichlar". Giyohvand moddalarni ishlab chiqarishda bioekvivalentlikni o'rganish: usullari va qo'llanilishi. Amaliyotda statistika. Chichester, Buyuk Britaniya: John Wiley and Sons. 17-36 betlar. ISBN 978-0-470-09475-4. Olingan 21 aprel 2011.
- Chou, Sheyn-Chung; Liu, Jen-pei (2008 yil 15 oktyabr). Bioavailability va Bioequivalents tadqiqotlarini loyihalashtirish va tahlil qilish. Biostatistika seriyasi. 27 (3-nashr). FL: CRC Press. ISBN 978-1-58488-668-6.


