Dori almashinuvi - Drug metabolism
Dori almashinuvi bu metabolik buzilish ning giyohvand moddalar yashash orqali organizmlar, odatda ixtisoslashgan orqali fermentativ tizimlar. Umuman olganda, ksenobiotik metabolizm (yunon tilidan ksenolar "notanish" va biotik "tirik mavjudotlar bilan bog'liq") to'plamidir metabolik yo'llar ning kimyoviy tuzilishini o'zgartiradigan ksenobiotiklar, bu organizmning normal biokimyosiga begona birikmalar, masalan, har qanday dori yoki zahar. Ushbu yo'llar biotransformatsiya organizmlarning barcha asosiy guruhlarida mavjud va qadimiy kelib chiqishi deb hisoblanadi. Ushbu reaktsiyalar ko'pincha harakat qiladi zararsizlantirish zaharli birikmalar (ba'zi hollarda bo'lsa ham oraliq mahsulotlar ksenobiotik metabolizmada o'zlari toksik ta'sirga olib kelishi mumkin). Dori almashinuvini o'rganish deyiladi farmakokinetikasi.
Ning metabolizmi farmatsevtik dorilar ning muhim jihati hisoblanadi farmakologiya va Dori. Masalan, metabolizm darajasi preparatning farmakologik ta'sirining davomiyligi va intensivligini belgilaydi. Dori almashinuvi ham ta'sir qiladi ko'p dori-darmonlarga qarshilik yilda yuqumli kasalliklar va kimyoviy terapiya uchun saraton va ba'zi dorilarning harakatlari substratlar yoki inhibitörler Ksenobiotik metabolizmda ishtirok etadigan fermentlarning zararli sababi hisoblanadi dorilarning o'zaro ta'siri. Ushbu yo'llar ham muhimdir ekologik fan, ning ksenobiotik metabolizmi bilan mikroorganizmlar davomida ifloslantiruvchi moddalarning parchalanishini aniqlash bioremediatsiya, yoki davom eting muhitda. Ksenobiotik metabolizmning fermentlari, xususan glutation S-transferazlar qishloq xo'jaligida ham muhimdir, chunki ular qarshilik ko'rsatishi mumkin pestitsidlar va gerbitsidlar.
Dori almashinuvi uch bosqichga bo'linadi. I fazada kabi fermentlar sitoxrom P450 oksidazalar ksenobiotiklarga reaktiv yoki qutbli guruhlarni kiritish. Ushbu modifikatsiyalangan birikmalar keyinchalik II bosqich reaktsiyalarida qutbli birikmalar bilan konjuge qilinadi. Ushbu reaktsiyalar katalizlanadi transferaza kabi fermentlar glutation S-transferazlar. Va nihoyat, III bosqichda konjuge ksenobiotiklar tan olinmasdan oldin qo'shimcha ravishda qayta ishlanishi mumkin oqimli transportyorlar va hujayralardan chiqarildi. Giyohvand moddalar almashinuvi ko'pincha o'zgaradi lipofil ichiga birikmalar hidrofilik osonroq bo'lgan mahsulotlar chiqarilgan.
O'tkazuvchanlik to'siqlari va zararsizlantirish
Organizm ta'sir qiladigan aniq birikmalar asosan oldindan aytib bo'lmaydi va vaqt o'tishi bilan juda katta farq qilishi mumkin; bu ksenobiotik toksik stressning asosiy xususiyatlari.[1] Ksenobiotik detoksifikatsiya tizimlari oldida turgan asosiy muammo shundaki, ular normal tarkibida bo'lgan kimyoviy moddalar aralashmasidan deyarli cheksiz ksenobiotik birikmalarni olib tashlashga qodir. metabolizm. Ushbu muammoni hal qilish uchun rivojlangan echim - bu jismoniy to'siqlar va past o'ziga xoslikning oqlangan kombinatsiyasi fermentativ tizimlar.
Barcha organizmlar foydalanadilar hujayra membranalari ularning ichki muhitiga kirishni boshqarish uchun gidrofobik o'tkazuvchanlik to'siqlari sifatida. Qutbiy birikmalar ular bo'ylab tarqalib keta olmaydi hujayra membranalari va foydali molekulalarni qabul qilish vositachilik qiladi transport oqsillari hujayra tashqari aralashmasidan maxsus substratlarni tanlaydigan. Ushbu tanlab olish eng ko'p narsani anglatadi hidrofilik molekulalar hujayralarga kira olmaydi, chunki ular biron bir transport vositasi tomonidan tan olinmagan.[2] Aksincha, diffuziya hidrofob Ushbu to'siqlar bo'ylab birikmalar boshqarilishi mumkin emas va shuning uchun organizmlar ularni istisno qila olmaydi lipid - membrana to'siqlaridan foydalangan holda eriydigan ksenobiotiklar.
Biroq, o'tkazuvchanlik to'sig'ining mavjudligi, organizmlar membrana o'tkazuvchan ksenobiotiklar uchun umumiy bo'lgan hidrofobiklikdan foydalanadigan detoksifikatsiya tizimlarini rivojlantira olishini anglatadi. Shuning uchun ushbu tizimlar deyarli har qanday qutblanmagan birikmani metabolizm qiladigan keng substrat xususiyatlariga ega bo'lish orqali o'ziga xoslik muammosini hal qiladi.[1] Foydali metabolitlar qutblanganligi sababli chiqarib tashlanadi va umuman bir yoki bir nechta zaryadlangan guruhlarni o'z ichiga oladi.
Oddiy metabolizmning reaktiv yon mahsulotlarini zararsizlantirishga yuqorida ko'rsatilgan tizimlar tomonidan erishib bo'lmaydi, chunki bu turlar oddiy uyali tarkibiy qismlardan kelib chiqadi va odatda qutb xususiyatlariga ega. Ammo, bu birikmalar oz sonli bo'lgani uchun, ma'lum fermentlar ularni tanib olib tashlashi mumkin. Ushbu o'ziga xos detoksifikatsiya tizimlariga misollar glyoksalaza tizimi, bu reaktivni olib tashlaydi aldegid metilglikoksal,[3] va yo'q qiladigan turli xil antioksidant tizimlar reaktiv kislorod turlari.[4]
Detoksifikatsiya bosqichlari
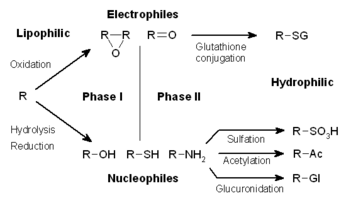
Ksenobiotiklarning metabolizmi ko'pincha uch bosqichga bo'linadi: - modifikatsiya, konjugatsiya va ajralish. Ushbu reaktsiyalar ksenobiotiklarni zararsizlantirish va hujayralardan olib tashlash uchun birgalikda harakat qiladi.
I bosqich - modifikatsiya
I fazada turli fermentlar reaktiv va qutbli guruhlarni substratlariga kiritish uchun harakat qiladi. Eng keng tarqalgan modifikatsiyalardan biri bu katalizatsiyalangan gidroksillanishdir sitoxrom P-450 ga bog'liq bo'lgan aralash funktsiyali oksidaz tizimi. Ushbu ferment komplekslari faollashtirilmagan uglevodorodlarga kislorod atomini kiritish uchun harakat qiladi, natijada ular gidroksil guruhlarini kiritishi yoki substratlarning N-, O- va S-dekkillanishiga olib kelishi mumkin.[5] P-450 oksidazlarning reaksiya mexanizmi quyidagi sxema bo'yicha sitoxrom bilan bog'langan kislorodni kamaytirish va yuqori reaktiv oksiferril turini yaratish orqali amalga oshiriladi:[6]
- O2 + NADPH + H+ + RH → NADP+ + H2O + ROH
I faza reaktsiyalari (shuningdek, ularni sintetik bo'lmagan reaktsiyalar deb ham atashadi) oksidlanish, kamaytirish, gidroliz, siklizatsiya, dekislizatsiya, va ko'pincha jigarda aralash funktsiyali oksidazlar tomonidan amalga oshiriladigan kislorod qo'shilishi yoki vodorodning chiqarilishi. Ushbu oksidlanish reaktsiyalari odatda a ni o'z ichiga oladi sitoxrom P450 monooksigenaza (ko'pincha qisqartirilgan CYP), NADPH va kislorod. Ushbu usuldan metabolizm uchun foydalanadigan farmatsevtik preparatlar sinflari kiradi fenotiyazinlar, paratsetamol va steroidlar. Agar I faza reaktsiyalarining metabolitlari etarlicha qutbli bo'lsa, ular shu vaqtda osongina chiqarilishi mumkin. Shu bilan birga, I fazali ko'plab mahsulotlar tezda yo'q qilinmaydi va keyingi reaksiyaga kirishadi, unda an endogen substrat yuqori darajada shakllantirish uchun yangi kiritilgan funktsional guruh bilan birlashadi qutbli konjugat.
I-bosqichdagi umumiy oksidlanish C-H bog'lanishining C-OH ga aylanishini o'z ichiga oladi. Ushbu reaktsiya ba'zida farmakologik jihatdan faol bo'lmagan birikmani o'zgartiradi (a oldingi dori ) farmakologik faolga. Xuddi shu asosda, I bosqich zaharli bo'lmagan molekulani zaharli moddaga aylantirishi mumkin (zaharlanish ). Oshqozon ichidagi oddiy gidroliz odatda zararsiz reaktsiya hisoblanadi, ammo istisnolar mavjud. Masalan, I fazadagi metabolizm aylanadi asetonitril HOCHga2Ichiga tez ajraladigan CN formaldegid va siyanid vodorodi.[7]
Preparat nomzodlarining metabolizmining I bosqichini laboratoriyada ferment bo'lmagan katalizatorlar yordamida simulyatsiya qilish mumkin.[8] Ushbu misol a biomimetik reaktsiya ko'pincha I fazali metabolitlarni o'z ichiga olgan mahsulotlarni berishga intiladi. Masalan, farmatsevtikaning asosiy metaboliti trimebutin, desmethyltrimebutine (nor-trimebutine), sotuvda mavjud bo'lgan preparatning in vitro oksidlanishi bilan samarali ishlab chiqarilishi mumkin. N-metil guruhining gidroksillanishi molekulaning chiqarilishiga olib keladi formaldegid, O-metil guruhlarining oksidlanishi kamroq darajada sodir bo'lganda.
Oksidlanish
- Sitoxrom P450 monooksigenaza tizimi
- Flavin tarkibidagi monooksigenaza tizimi
- Alkogolli dehidrogenaza va aldegid dehidrogenaza
- Monoamin oksidaz
- Birgalikda oksidlanish peroksidazlar
Kamaytirish
Sitokrom P450 reduktaza, shuningdek NADPH: ferrihemoprotein oksidoreduktaza, NADPH: gemoprotein oksidoreduktaza, NADPH: P450 oksidoreduktaza, P450 reduktaza, POR, CPR, CYPOR, sitokning elektroni mikroorganizmlar uchun zarur bo'lgan membrana bilan bog'langan fermentdir. FAD va FMN o'z ichiga olgan NADPH fermentidan olingan hujayra: sitokrom P450 reduktaza POR / P450 tizimidagi elektron oqimining umumiy sxemasi: NADPH → FAD → FMN → P450 → O2
Reduksiya reaktsiyalari paytida kimyoviy moddalar kirishi mumkin befoyda velosiped, unda erkin radikalli elektronga ega bo'ladi, keyin darhol uni yo'qotadi kislorod (shakllantirish uchun superoksid anion ).
Gidroliz
II bosqich - konjugatsiya
Keyingi II bosqich reaktsiyalarida bu faollashtirilgan ksenobiotik metabolitlar uyg'unlashgan kabi zaryadlangan turlari bilan glutation (GSH), sulfat, glitsin, yoki glyukuron kislotasi. Konjugatsiya reaktsiyalari paydo bo'ladigan dorilarning saytlariga quyidagilar kiradi karboksil (-COOH), gidroksil (-OH), amino (NH2) va sulfhidril (-SH) guruhlari. Konjugatsiya reaktsiyalari mahsulotlari molekula massasini ko'paytirdi va substratlarga qaraganda kamroq faol bo'ladi, aksariyat hollarda hosil bo'ladigan I bosqich reaktsiyalaridan farq qiladi. faol metabolitlar. Katta anion guruhlarining qo'shilishi (masalan, GSH) reaktivni zararsizlantiradi elektrofillar va membranalar bo'ylab tarqalib ketmaydigan ko'proq qutbli metabolitlarni ishlab chiqaradi va shuning uchun ularni faol ravishda tashish mumkin.
Ushbu reaktsiyalar keng spesifiklikdagi transferazlarning katta guruhi tomonidan katalizlanadi, ular kombinatsiyada nukleofil yoki elektrofil guruhlarni o'z ichiga olgan deyarli har qanday hidrofob birikmani metabolizm qilishi mumkin.[1] Ushbu guruhning eng muhim sinflaridan biri bu glutation S-transferazlar (GST).
| Mexanizm | Ishtirok etgan ferment | Ko-omil | Manzil | Manbalar |
|---|---|---|---|---|
| metilatsiya | metiltransferaza | S-adenosil-L-metionin | jigar, buyrak, o'pka, CNS | [9] |
| sulfatlash | sulfotransferazlar | 3'-fosfoadenozin-5'-fosfosulfat | jigar, buyrak, ichak | [9] |
| atsetilatsiya | atsetil koenzim A | jigar, o'pka, taloq, oshqozon shilliq qavati, RBClar, limfotsitlar | [9] | |
| glyukuronidatsiya | UDP-glyukuronosiltransferazlar | UDP-glyukuron kislotasi | jigar, buyrak, ichak, o'pka, teri, prostata, miya | [9] |
| glutation konjugatsiyasi | glutation S-transferazlar | glutation | jigar, buyrak | [9] |
| glitsin konjugatsiyasi | Ikki bosqichli jarayon:
| glitsin | jigar, buyrak | [10] |
III bosqich - keyingi modifikatsiya va ajralib chiqish
II bosqich reaktsiyalaridan so'ng, ksenobiotik konjugatlar yana metabolizmga uchrashi mumkin. Umumiy misol - glutation konjugatlarini qayta ishlash asetilsistein (merkapturik kislota) konjugatlari.[11] Mana b-glutamat va glitsin glutation molekulasidagi qoldiqlar tomonidan olib tashlanadi Gamma-glutamil transpeptidaza va dipeptidazlar. Oxirgi bosqichda sistin konjugatdagi qoldiq atsetillangan.
Konjugatlar va ularning metabolitlari metabolizmning III fazasida hujayralardan chiqarilishi mumkin, shu bilan birga anion guruhlari membranalarning turli xil tashuvchilariga yaqinlik yorlig'i vazifasini bajaradi. ko'p dori-darmonlarga qarshilik ko'rsatadigan oqsil (MRP) oilasi.[12] Ushbu oqsillar oila a'zolari ATP bilan bog'laydigan kassetali transportyorlar va turli xil gidrofob anionlarning ATP ga bog'liq transportini katalizatsiyalashi mumkin,[13] va shu tariqa II fazali mahsulotlarni hujayradan tashqaridagi muhitga olib tashlash uchun harakat qiling, bu erda ular qo'shimcha metabolizmga yoki tashqariga chiqarilishi mumkin.[14]
Endogen toksinlar
Kabi endogen reaktiv metabolitlarning zararsizlantirilishi peroksidlar va reaktiv aldegidlar ko'pincha yuqorida tavsiflangan tizim tomonidan erishib bo'lmaydi. Bu ushbu turlarning normal uyali tarkibiy qismlardan olinishi va odatda qutb xususiyatlarini bo'lishishining natijasidir. Ammo, bu birikmalar soni kam bo'lganligi sababli, fermentativ tizimlar ularni tanib olish va yo'q qilish uchun o'ziga xos molekulyar tanib olishdan foydalanishlari mumkin. Ushbu molekulalarning foydali metabolitlarga o'xshashligi, shuning uchun har bir endogen toksinlar guruhining metabolizmi uchun odatda turli xil detoksifikatsiya fermentlari zarurligini anglatadi. Ushbu o'ziga xos detoksifikatsiya tizimlariga misollar glyoksalaza tizimi reaktiv aldegidni yo'q qilish uchun harakat qiladi metilglikoksal va turli xil antioksidant o'chiradigan tizimlar reaktiv kislorod turlari.
Saytlar
Miqdoriy ravishda silliq endoplazmatik to'r ning jigar hujayra dori metabolizmining asosiy organidir, ammo har biri biologik to'qima Jigarning dori metabolizmiga qo'shadigan hissasi uchun javobgar bo'lgan omillarga uning katta organ ekanligi, u tarkibiga singib ketgan kimyoviy moddalar tomonidan singdirilgan birinchi organ kiradi. ichak va boshqa metabolizmga uchragan ferment tizimlarining ko'pchiligining boshqa organlarga nisbatan juda yuqori konsentratsiyasi bor, agar preparat GI traktiga qabul qilinsa, u orqali jigar aylanishiga kiradi. portal tomir, u yaxshi metabolizmga uchraydi va deyiladi birinchi o'tish effekti.
Dori almashinuvining boshqa joylariga quyidagilar kiradi epiteliya hujayralari ning oshqozon-ichak trakti, o'pka, buyraklar, va teri Ushbu saytlar odatda mahalliy toksik reaktsiyalar uchun javobgardir.
Dori almashinuviga ta'sir qiluvchi omillar
Ko'pgina lipofil preparatlarining farmakologik ta'sirining davomiyligi va intensivligi ular faol bo'lmagan mahsulotlarga metabolizm darajasi bilan belgilanadi. Sitoxrom P450 monooksigenaza tizimi bu boradagi eng muhim yo'ldir. Umuman olganda ortadi metabolizm darajasi (masalan., fermentlar induksiyasi ) farmakologik faol metabolitning irodasi pasayish dori ta'sirining davomiyligi va intensivligi, aksincha (masalan., fermentlarni inhibatsiyasi ). Shu bilan birga, ferment pro-preparatni metabolizmga mas'ul bo'lgan holatlarda, ferment induksiyasi bu konversiyani tezlashtirishi va giyohvand moddalar miqdorini oshirishi, toksikani keltirib chiqarishi mumkin.
Turli xil fiziologik va patologik Dori almashinuviga ta'sir etuvchi fiziologik omillarga yosh, individual o'zgarish kiradi (masalan., farmakogenetika ), enterohepatik qon aylanishi, oziqlanish, ichak florasi, yoki jinsiy farqlar.
Umuman olganda, dorilar sekinroq metabollanadi homila, yangi tug'ilgan chaqaloq va qariyalar odamlar va hayvonlar ga qaraganda kattalar.
Genetika o'zgarishi (polimorfizm ) dorilar ta'siridagi ba'zi o'zgaruvchanlikni hisobga oladi. N-asetiltransferazlar bilan (tarkibiga kiradi) II bosqich reaktsiyalar), individual o'zgaruvchanlik asta-sekin atsetilat qiladigan odamlar guruhini yaratadi (sekin atsetilatorlar) va atsetilat bilan tezda shug'ullanadiganlar taxminan 50:50 populyatsiyada bo'linadi Kanada.Bu xilma-xillik dramatik oqibatlarga olib kelishi mumkin sekin atsetilatorlar dozaga bog'liq toksikaga ko'proq moyil.
Sitoxrom P450 monooksigenaza tizimi fermentlar individual ravishda ham farq qilishi mumkin, etishmovchilik ularning etnik kelib chiqishiga qarab odamlarning 1-30 foizida uchraydi.
Preparatning dozasi, chastotasi, qabul qilish usuli, to'qimalarning tarqalishi va oqsil bilan bog'lanishi uning metabolizmiga ta'sir qiladi.
Patologik omillar shuningdek, giyohvand moddalar almashinuviga ta'sir qilishi mumkin jigar, buyrak, yoki yurak kasalliklar.
Silikonda modellashtirish va simulyatsiya usullari odamlarda klinik tadqiqotlar o'tkazilishidan oldin virtual bemor populyatsiyalarida dori metabolizmini taxmin qilish imkonini beradi.[15] Bu nojo'ya reaktsiya xavfi yuqori bo'lgan shaxslarni aniqlash uchun ishlatilishi mumkin.
Tarix
Odamlar o'zlariga yutadigan moddalarni qanday o'zgartirishi bo'yicha tadqiqotlar XIX asrning o'rtalarida boshlandi, kimyogarlar bu kabi organik kimyoviy moddalarni topdilar. benzaldegid inson organizmidagi aminokislotalarga oksidlanib, konjuge bo'lishi mumkin.[16] O'n to'qqizinchi asrning qolgan davrida, boshqa bir qator asosiy detoksifikatsiya reaktsiyalari topildi, masalan metilatsiya, atsetilatsiya va sulfanlash.
Yigirmanchi asrning boshlarida, ushbu metabolitlarni ishlab chiqarish uchun mas'ul bo'lgan fermentlar va yo'llarni tekshirishga kirishildi. Ushbu soha tomonidan nashr etilgan holda alohida tadqiqot yo'nalishi sifatida aniqlandi Richard Uilyams kitobning Detoksikatsiya mexanizmlari 1947 yilda.[17] Ushbu zamonaviy biokimyoviy tadqiqotlar natijasida glutation aniqlandi S- 1961 yilda o'tkazilgan transferlar,[18] keyin 1962 yilda sitoxrom P450s kashf qilindi,[19] va ularning 1963 yilda ksenobiotik metabolizmdagi asosiy rolini anglash.[20][21]
Shuningdek qarang
Adabiyotlar
- ^ a b v Jakoby WB, Ziegler DM (dekabr 1990). "Detoksikatsiya fermentlari". J. Biol. Kimyoviy. 265 (34): 20715–8. PMID 2249981.
- ^ Mizuno N, Niwa T, Yotsumoto Y, Sugiyama Y (sentyabr 2003). "Dori-darmonlarni tashuvchilarni tadqiq qilishning dori-darmonlarni topish va rivojlanishiga ta'siri". Farmakol. Vah. 55 (3): 425–61. doi:10.1124 / pr.55.3.1. PMID 12869659. S2CID 724685.
- ^ Thornalley PJ (1990 yil iyul). "Glyoksalaza tizimi: biologik hayot uchun metabolik yo'lni funktsional tavsiflash bo'yicha yangi o'zgarishlar". Biokimyo. J. 269 (1): 1–11. doi:10.1042 / bj2690001. PMC 1131522. PMID 2198020.
- ^ Sies H (mart 1997). "Oksidlanish stressi: oksidlovchilar va antioksidantlar" (PDF). Muddati Fiziol. 82 (2): 291–5. doi:10.1113 / expphysiol.1997.sp004024. PMID 9129943. Arxivlandi asl nusxasi (PDF) 2009-03-25. Olingan 2012-12-29.
- ^ Guengerich FP (iyun 2001). "Metabolizm va kimyoviy toksiklik bilan bog'liq bo'lgan umumiy va kam uchraydigan sitoxrom P450 reaktsiyalari". Kimyoviy. Res. Toksikol. 14 (6): 611–50. doi:10.1021 / tx0002583. PMID 11409933.
- ^ Schlichting I, Berendzen J, Chu K, Stock AM, Maves SA, Benson DE, Sweet RM, Ringe D, Petsko GA, Sligar SG (2000 yil mart). "Atom piksellar soniga p450cam sitoxromining katalitik yo'li". Ilm-fan. 287 (5458): 1615–22. Bibcode:2000Sci ... 287.1615S. doi:10.1126 / science.287.5458.1615. PMID 10698731.
- ^ "Asetonitril (EHC 154, 1993)". www.inchem.org. Olingan 2017-05-03.
- ^ Akagah B, Lormier AT, Fournet A, Figadère B (dekabr 2008). "Metalloporfirin katalizatorlaridan foydalangan holda antiparazitik 2-o'rnini bosuvchi kinolinlarni oksidlash: preparat nomzodlarining metabolitlarini ishlab chiqarish uchun biomimetik reaktsiyani kattalashtirish". Org. Biomol. Kimyoviy. 6 (24): 4494–7. doi:10.1039 / b815963g. PMID 19039354.
- ^ a b v d e Liston HL, Markovits JS, DeVane CL (oktyabr 2001). "Klinik psixofarmakologiyada dori glyukuronidatsiyasi". J Clin Psixofarmakol. 21 (5): 500–15. doi:10.1097/00004714-200110000-00008. PMID 11593076. S2CID 6068811.
- ^ Badenhorst CP, van der Sluis R, Erasmus E, van Deyk AA (2013 yil sentyabr). "Glisin konjugatsiyasi: metabolizmdagi ahamiyati, glitsin N-asiltransferazaning roli va shaxslararo o'zgarishga ta'sir qiluvchi omillar". Giyohvand moddalar almashinuvi va toksikologiya bo'yicha mutaxassislarning fikri. 9 (9): 1139–1153. doi:10.1517/17425255.2013.796929. PMID 23650932. S2CID 23738007.
Glisin N-asiltransferaza (GLYAT, E.C. 2.3.1.13) tomonidan katalizlangan mitoxondriyal asil-KoAlarning glitsin konjugatsiyasi etarli miqdordagi erkin koenzim A (CoASH) ni saqlash uchun javob beradigan muhim metabolik yo'ldir. Ammo, glitsin bilan biriktirilgan farmatsevtika preparatlari kamligi sababli, yo'l hali batafsil tavsiflanmagan. Bu erda biz glitsin konjugatsiya yo'lidagi shaxslararo o'zgarishning sabablari va mumkin bo'lgan oqibatlarini ko'rib chiqamiz. ...
Shakl 1. Benzo kislotasining glitsin konjugatsiyasi. Glitsin konjugatsiya yo'li ikki bosqichdan iborat. Birinchi benzoat yuqori energiyali benzoil-CoA tioesterini hosil qilish uchun CoASH bilan bog'lanadi. Ushbu reaktsiya HXM-A va HXM-B o'rta zanjirli kislota: CoA ligazlari bilan katalizlanadi va ATP shaklida energiya talab qiladi. ... Keyin benzoil-CoA GLYAT bilan glitsinga konjugatsiya qilinadi va gipur kislotasini hosil qiladi va CoASH ni chiqaradi. Qutilarda sanab o'tilgan omillardan tashqari ATP, CoASH va glitsin darajalari glitsin konjugatsiya yo'lining umumiy tezligiga ta'sir qilishi mumkin. - ^ Boyland E, Chasseaud LF (1969). "Merkapturik kislota biosintezida glutation va glutation S-transferazlarning roli". Adv. Ferment. Relat. Mollar. Biol. Enzimologiya yutuqlari - va molekulyar biologiyaning tegishli sohalari. 32: 173–219. doi:10.1002 / 9780470122778.ch5. ISBN 9780470122778. PMID 4892500.
- ^ Homolya L, Varadi A, Sarkadi B (2003). "Ko'p dori-darmonlarga qarshilik bilan bog'liq oqsillar: glutation, glyukuronat yoki sulfat bilan konjugatlar uchun eksport nasoslari". BioFaktorlar. 17 (1–4): 103–14. doi:10.1002 / biof.5520170111. PMID 12897433. S2CID 7744924.
- ^ König J, Nies AT, Cui Y, Leier I, Keppler D (dekabr 1999). "Ko'p dori-darmonlarga chidamli oqsil (MRP) oilasining konjugat eksport nasoslari: lokalizatsiya, substratning o'ziga xosligi va MRP2 vositachiligida dori-darmonlarga qarshilik". Biokimyo. Biofiz. Acta. 1461 (2): 377–94. doi:10.1016 / S0005-2736 (99) 00169-8. PMID 10581368.
- ^ Qo'mondon JN, Stijntjes GJ, Vermeulen NP (iyun 1995). "Glyutation S-konjugatlarining hosil bo'lishi va joylashtirilishida ishtirok etadigan fermentlar va transport tizimlari. Ksenobiotiklarning bioaktivatsiyasi va zararsizlantirish mexanizmlarining ahamiyati". Farmakol. Vah. 47 (2): 271–330. PMID 7568330.
- ^ Rostami-Xodjegan A, Taker GT (2007 yil fevral). Inson populyatsiyasida in vivo jonli ravishda metabolizmni simulyatsiya qilish va bashorat qilish in vitro ma'lumotlar ". Nat Rev Drug Discov. 6 (2): 140–8. doi:10.1038 / nrd2173. PMID 17268485. S2CID 205476485.
- ^ Murphy PJ (iyun 2001). "Ksenobiotik metabolizm: o'tmishdan kelajakka qarash". Dori vositasi. Disposlar. 29 (6): 779–80. PMID 11353742.
- ^ Neuberger A, Smit RL (1983). "Richard Tekvin Uilyams: odam, uning ishi, uning ta'siri". Dori vositasi. Vah. 14 (3): 559–607. doi:10.3109/03602538308991399. PMID 6347595.
- ^ Booth J, Boyland E, Sims P (1961 yil iyun). "Glutation bilan konjugatsiyani katalizlovchi kalamush jigaridan ferment". Biokimyo. J. 79 (3): 516–24. doi:10.1042 / bj0790516. PMC 1205680. PMID 16748905.
- ^ Omura T, Sato R (1962 yil aprel). "Jigar mikrosomalaridagi yangi sitoxrom". J. Biol. Kimyoviy. 237: 1375–6. PMID 14482007.
- ^ Estabrook RW (2003 yil dekabr). "P450-larga bo'lgan ehtiros (P450 sitokromi bo'yicha dastlabki tadqiqotlar tarixining esdaliklari)". Dori vositasi. Disposlar. 31 (12): 1461–73. doi:10.1124 / dmd.31.12.1461. PMID 14625342.
- ^ Estabrook RW, Cooper DY, Rosenthal O (1963). "Buyrak usti korteksidagi steroid C-21 gidroksilaza tizimining engil qaytariladigan uglerod oksidi inhibatsiyasi". Biokimyo Z. 338: 741–55. PMID 14087340.
Qo'shimcha o'qish
- Parvez H, Reiss C (2001). Ksenobiotiklarga molekulyar javoblar. Elsevier. ISBN 0-345-42277-5.
- Ioannides C (2001). Dori-darmonlarni va boshqa ksenobiotiklarni metabolizadigan ferment tizimlari. John Wiley va Sons. ISBN 0-471-89466-4.
- Richardson M (1996). Atrof-muhit ksenobiotikalari. Teylor va Frensis Ltd. ISBN 0-7484-0399-X.
- Ioannides C (1996). Sitoxromlar P450: metabolik va toksikologik jihatlar. CRC Press Inc. ISBN 0-8493-9224-1.
- Avasthi YC (2006). Glutationin S-transfertlarining toksikologiyasi. CRC Press Inc. ISBN 0-8493-2983-3.
Tashqi havolalar
- Ma'lumotlar bazalari
- Dori almashinuvi
- Mikrobial biodegradatsiya
- Tarix
- Ksenobiotik metabolizm tarixi da Orqaga qaytish mashinasi (arxivlangan 2007 yil 13-iyul)
