Periferik ta'sir qiluvchi m-opioid retseptorlari antagonisti - Peripherally acting μ-opioid receptor antagonist
Periferik harakat qiladi m-opioid retseptorlari antagonistlar (PAMORA) - sinf kimyoviy birikmalar orqaga qaytarish uchun ishlatiladi salbiy ta'sir sabab bo'lgan opioidlar bilan o'zaro aloqada bo'lish retseptorlari tashqarida markaziy asab tizimi (CNS), asosan oshqozon-ichak trakti. PAMORA'lar ma'lum narsalarga to'sqinlik qilish uchun mo'ljallangan opioid retseptorlari oshqozon-ichak traktida va o'tish qobiliyati cheklangan qon-miya to'sig'i. Shuning uchun, PAMORA'lar ta'sir qilmaydi og'riq qoldiruvchi markaziy asab tizimidagi opioidlarning ta'siri.[1]
Kashfiyot va rivojlanish
Opioid preparatlari sabab bo'lishi ma'lum opioid ta'sirida ich qotishi (OIC) inhibisyon bilan oshqozonni bo'shatish va kamayadi peristaltik dori-darmonlarni so'rilishini kechiktirishga olib keladigan to'lqinlar va najas. Buning natijasida qattiq va quruq najas va ich qotishi ba'zi bemorlar uchun.[2]
IHT eng keng tarqalganlardan biridir salbiy ta'sir opioidlar tomonidan kelib chiqqan, shuning uchun PAMORA-larning kashf etilishi ko'pincha buziladigan ta'sirlarning oldini oladi og'riqni davolash.[3]
Metilnaltrekson bromidi ichidagi birinchi dori edi giyohvand moddalar sinfi tomonidan tasdiqlangan FDA.[4] Uni 1979 yilda Leon Goldberg, a farmakolog da Chikago universiteti. Iqtisodiy hamkorlik bilan o'layotgan do'stining azoblanishiga guvoh bo'lgan Goldberg har xil sinovlarni o'tkazdi hosilalar ning naltrekson, opioidlarning ta'sirini blokirovka qilish uchun ma'lum bo'lgan dori. Uning maqsadi dorini o'tolmaydigan dorini topish edi qon-miya to'sig'i, opioidlarning og'riq qoldiruvchi ta'siriga ta'sir qilmasdan. Goldberg vafot etganidan so'ng, uning universitetdagi hamkasblari birikmani ishlab chiqarishni davom ettirdilar. U 2008 yil aprel oyida FDA tomonidan tasdiqlangan, dastlab OIC uchun, rivojlangan kasalligi bo'lgan kattalar bemorlarida va keyinchalik surunkali saraton kasalligi bilan og'rigan kattalar bemorlarida.[5]
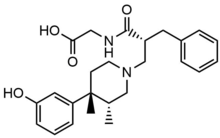
1970-yillarning oxirida Dennis M. Zimmerman va uning hamkasblari Lilly tadqiqot laboratoriyalari, Indiana, 4-fenilpiperidin seriyasida aniqlangan giyohvandlik antagonistlari uchun strukturaviy tushunchalar bo'yicha tadqiqotlar o'tkazdi.[6] Ular xabar berishdi N-metil-trans-3,4-dimetil-4-fenilpiperidin toza opioid retseptorlari antagonist yangi bilan farmakofor. Oshirish uchun kuch ular biriktirilgan fenolik guruh uchun aromatik halqa, N-metil-trans-3,4-dimetil-4- (3-gidroksifenil) piperidin. Ushbu tuzilish, masalan, boshqa opioid retseptorlari antagonistlarini ishlab chiqish va rivojlantirish uchun ishlatilgan alvimopan.[5] Alvimopan 2008 yilda kasalxonada davolanishni oshirish uchun tasdiqlangan oshqozon-ichak trakti faoliyati qisman katta yoki ingichka ichak rezektsiya birlamchi anastomoz. Naloksegol 2014 yil sentyabr oyida tasdiqlangan va naldemedin 2017 yil mart oyida ikkala surunkali saraton kasalligiga chalingan kattalardagi bemorlarda OICni davolash uchun.[7][8][9][10]
Ta'sir mexanizmi
PAMORAlar opioidlarning bog'lanishiga to'sqinlik qiladi agonist uchun m-opioid retseptorlari (MOR). PAMORAni davolashning maqsadi qayta tiklashdir ichak asab tizimi funktsiyasi (ENS). MOR tanadagi bir nechta joylarda uchraydi va PAMORAlar a raqobatdosh antagonist retseptor bilan bog'lanish uchun. Oshqozon-ichak traktidagi MORlar PAMORA-lar opioid agonistlarini bog'lash va oldini olish uchun mo'ljallangan asosiy retseptorlardir.[11] PAMORAlar opioid bilan bog'liq ichak disfunktsiyasini (OIBD) davolashda ishlatiladi, bu surunkali opioiddan kelib chiqadigan salbiy ta'sir. PAMORAlar uchtasida harakat qilishadi patofizyolojik ushbu salbiy ta'sir mexanizmlari. Ular harakat qilishadi ichak harakatlanishi, ichak sekretsiyasi va sfinkter funktsiya.[12]
PAMORA ning ichak harakatiga ta'siri shundaki, u dumaloq mushak qavatida dam olish ohangini oshirishi mumkin. Antagonist tonik inhibisyoniga ta'sirini kuchaytiradi mushak tonusi. Bu dumaloq mushak qavatidagi ohangni normallashtiradi va shuning uchun opioid ta'sirida ritmik qisqarishning oldini oladi. Ushbu ikki omil birlashganda, bu pasayishiga olib keladi tranzit vaqti. Ushbu ta'sir suyuqliklarning passiv singishini pasaytiradi, bu esa ich qotish kabi OIBD belgilarining pasayishiga yordam beradi. ichak spazmi va qorin kramplari.[13]
PAMORA ning ichak sekretsiyasiga ta'siri pasayganlikni qaytarishga yordam beradi lager opioid agonistlari keltirib chiqaradigan shakllanish.[14] Shuningdek, antagonist odatdagi sekretsiyani o'rnatadi xlorid. Opioidlar agonistlari ham kamaytirishi mumkin sekretsiya ning peptidlar oshirish orqali simpatik asab tizimi quruqroq va qattiqroq najasga olib kelishi mumkin bo'lgan ENSdagi m-retseptorlari orqali. PAMORAlar unga qarshi ishlaydi, shuning uchun najas yumshoq va kamroq quriydi.[13]
PAMORA ning funktsiyasiga ta'siri sfinkter nazariyani harakatni muvofiqlashtirishni tartibga solishdir. Antagonist oldini olishi mumkin Oddi disfunktsiyasining sfinkteri bu opioidlardan kelib chiqadi.[15] Antagonistlar, shuningdek, opioid bilan bog'liq anal sfinkter disfunktsiyasini kamaytirishi mumkin. Disfunktsiya bog'liq zo'riqish, gemorroy va to'liq bo'lmagan bo'shatish.[16]
Tarkib va faoliyat munosabatlari
M-opioid retseptorlari (MOR) ga qaratilgan dorilar uzoq vaqt davomida ishlatilgan bo'lsa ham, bu haqda ko'p narsa ma'lum emas tuzilish-faoliyat munosabatlari va ligand -retseptorlarning o'zaro ta'siri aniq belgilangan asosda biologik ta'sir retseptorlari faollashishi yoki inhibatsiyasi to'g'risida. Shuningdek, agonistlar va antagonistlarning retseptorlari-ligandning o'zaro ta'sirining farqlari aniq ma'lum emas. Bir nazariya shuni ta'kidlaydi morfinanlar biologik faollikni N-o'rnini bosuvchi moddalarning kattaligi bilan aniqlash mumkin edi. Masalan, antagonistlar odatda katta o'rinbosarlarga ega, masalan allil - yoki siklopropil metil morfinli azotda, agonistlarda esa odatda a mavjud metil guruhi. Boshqa tomondan, agonist faollik morfin azotida katta guruhlarga ega ligandlarda ham ko'rsatiladi va shuning uchun bu gipotezaga qarshi chiqiladi.[17]
Tuzilishi

Metilnaltrekson bromidi, naloksegol va naldemedinning tuzilishi o'xshashdir, bu kimyoviy tuzilishidan unchalik uzoq emas. morfin va boshqa MOR-agonistlar. Barchasida qattiq narsa bor pentatsiklik o'z ichiga olgan tuzilish benzol halqasi (A), tetrahidrofuran uzuk (B), ikkitasi sikloheksan uzuklar (C va D) va a piperidin uzuk (E).[18] Opioidlarning biologik ta'siri uchun eng muhim funktsional guruhlar quyidagilardir gidroksil guruhi ustida fenol, N-metil guruhi, efir C4 va C5 orasidagi ko'prik, qo'shaloq bog'lanish o'rtasida uglerod C7 va C8 raqamlari va C3 va C6 da gidroksil guruhlari. Fenolik halqa va uning 3-gidroksil guruhi og'riq qoldiruvchi ta'sir uchun juda muhimdir, chunki OH guruhini olib tashlash analjezik faolligini 10 baravar kamaytiradi. C6 bo'yicha gidroksil guruhi uchun yana bir printsip mavjud, chunki olib tashlash uning faolligini oshiradi. Faoliyatning kuchayishi asosan kuchayganligi sababli lipofillik qon-miya to'sig'idan o'tish qobiliyatining oshishi. Naldemedin gidroksil guruhiga ega, metilnaltrekson bromid esa a ga ega keton guruh va naloksegol an Ester. Analjezik ta'sir uchun C7 va C8 orasidagi er-xotin bog'lanish talab qilinmaydi va er-xotin bog'lanishning kamayishi faollikni oshiradi. Antagonistlarning hech birining tuzilishida er-xotin bog'lanish mavjud emas. Skelet ustidagi N-substituent farmakologik xatti-harakatni va uning MOR bilan o'zaro ta'sirini aniqlaydi deb o'ylashadi. Shuningdek, antagonistlarni agonistlardan ajratishda asosiy rol o'ynaydi deb o'ylashadi. Alil guruhi, a metilsiklopropil guruhi yoki a metilsiklobutil chunki N-o'rnini bosuvchi guruhlar antagonist faollikni boshqaradi.[19][20][21]
Majburiy sayt
Agonistlar va antagonistlar aniqlik hosil qiladi kimyoviy aloqalar bilan aminokislotalar MORni quradigan. Antagonistlarning aksariyati, shuningdek agonistlar shakllanishi taxmin qilinmoqda zaryadlangan o'zaro ta'sir Asp147 va a bilan vodorod aloqasi Tyr148 bilan. Biroq, antagonistlarning aksariyati qo'shimcha ham hosil qiladi qutbli o'zaro ta'sirlar Lys233, Gln124, Gln229, Asn150, Trp318 va Tyr128 kabi boshqa aminokislota qoldiqlari bilan. Faqatgina ozgina agonistlar bir xil qo'shimcha qutbli o'zaro ta'sirlarni hosil qiladi. Ham agonistlar, ham antagonistlar His297 bilan vodorod aloqalarini hosil qilishi ma'lum.[22]
Asp147 va Tyr148 aminokislotalar qoldiqlari bilan o'zaro ta'sirlar ligand retseptorlari bilan bog'lanish va boshqa qoldiqlar bilan qo'shimcha qutbli o'zaro ta'sir hosil qiluvchi molekulalar agonistlarga qaraganda ko'pincha antagonistlardir.[17]
N-o'rnini bosuvchi guruh hosil bo'lishi mumkin hidrofob Tyr326 va Trp293 bilan bog'lanishlar va aromatik va sikloheksan halqalari Met151 ga o'xshash bog'lanishlarni hosil qilishi mumkin. Ligandning orqa tomoni ham hidrofob bog'lanish hosil qilishi mumkin, ammo Val300 va Ile296 bilan.[22]
Metilnaltrekson bromidi
Metilnaltrekson bromidi bu bromid metilnaltreksonning tuz shakli, a to'rtinchi davr ning metil hosilasi noroksimorfon. Metil guruhi va to'rtinchi tuz tuzilishi ortadi kutupluluk va kamaytirish lipidlarda eruvchanligi shu bilan qon-miya to'sig'ining kirib borishini cheklaydi. Metilnaltrekson sakkiz baravar yuqori qarindoshlik uchun MOR uchun b-opioid retseptorlari (KOR) va b-opioid retseptorlari (DOR).[23] Naltrekson Asp147 va Tyr148 bilan o'zaro ta'sir hosil qiladi vodorod aloqasi Lys233 bilan.[24]

Alvimopan

Periferik selektiv trans-3,4-dimetil-4- (3-gidroksilfenil) piperidin opioid antagonistlari davolash uchun ishlab chiqilgan oshqozon-ichak motorikasi Zimmerman va uning hamkasblari tomonidan tartibsizlik. Shundan kelib chiqib, ular 4- (3-gidroksifenil) -3,4-dimetilpiperidin iskala ishlab chiqarishni turli o'lchamlari, zaryadi va qutbliligini qamrab oluvchi funktsional guruhlar bilan birgalikda opioid retseptorlari antagonizmiga erishish uchun CNS dori ta'sirini kamaytirdilar. The in vitro m-Ki, jonli ravishda AD50 va ED50 va periferik indeks (nisbat) bir nechta selektiv analoglar uchun tekshirildi va shundan ular trans-3,4-dimetil-4- (3-gidroksifenil) piperidin Alvimopan eng yaxshi natijalarni berganligini aniqladilar.[5] Katta zvitterionik tuzilishi va yuqori kutupluluğu Alvimopanning qon-miya to'sig'idan o'tishiga to'sqinlik qiladi, shu bilan periferik MORlarni bog'lash kuchi markaziy MORlardan 200 baravar ko'pdir.[25]
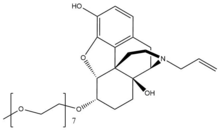
Naloksegol
Naloxegol a polietilen glikol a-ning modifikatsiyalangan hosilasinaloksol. Naloxegol shunga o'xshash shaklga ega nalokson kabi heteropentatsiklik ikkalasida ham an allil guruhi ga biriktirilgan omin ning piperidin uzuk. Ammo naloksegol monometoksi bilan tugagan n = 7 ga ega oligomer ning PEG b-naloksolning 6-alfa-gidroksil guruhiga an orqali ulangan efir bog'lanish. PEG qismi bu miqdorni oshiradi molekulyar og'irlik va shuning uchun naloksegolni qabul qilishni cheklaydi CNS.[26] Bundan tashqari, pegillangan naloksegol a ga aylanadi substrat uchun P-glikoprotein oqish birikmani CNS tashqarisiga olib chiqadigan transportyor.[27]
Naldemedin
Naldemedin naltreksonga o'xshash kimyoviy tuzilishga ega, ammo qo'shimcha yon zanjir bilan molekulyar og'irlik va qutb sirt maydoni moddaning Naloksegol singari naldemedin ham P-glikoprotein effluks tashuvchisi substratidir. Ushbu xususiyatlar CNSga kamroq kirib borishiga olib keladi va opioid agonistlari ta'sirida mumkin bo'lgan xulosani kamaytiradi.[28]Naldemedine MOR va DOR uchun dual antagonistdir. DOR ning faollashishi ko'ngil aynish va / yoki qayt qilishni keltirib chiqarishi ma'lum bo'lgan, shuning uchun dual antagonist OICni ham, ko'ngil aynishi / qayt qilishni ham kamaytirishi mumkin.[29]
Farmakokinetikasi
The molekulyar og'irlik, bioavailability, oqsil bilan bog'lanish, yarim umrni yo'q qilish, maksimal plazma kontsentratsiyasiga erishish vaqti va majburiy yaqinlik quyidagi jadvalda mavjud.[26][23]
| Kimyoviy nomi | Kimyoviy tuzilishi | Molekulyar og'irlik (g / mol) | Bioavailability (%) | Plazma oqsillari bilan bog'lanish (%) | t1/2 (h) | tmaksimal | Ki m (nM) | Ki κ (nM) | Ki δ (nM) |
|---|---|---|---|---|---|---|---|---|---|
| Metilnaltrekson bromid | 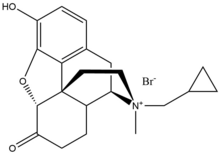 | 436,3 | Kam | 11-15 | 8 | 30 min | 5.50 | 32.1 | 3453.8 |
| Alvimopan |
| 424,53 | 6 | 80-90 | 10-17 | 2 soat | 0.77 | 40 | 4.4 |
| Naloksegol |
| 651,798 | NA | 4,2 | 6-11 | 2 soat | 7.42 | 8.65 | 203.0 |
| Naldemedin |
| 570,6 | 29 | 93-94 | 11 | 45 min | 0.34 | 0.94 | 0.43 |
- t1/2: Biologik yarim umr
- tmaksimal: Plazmadagi maksimal kontsentratsiyaga erishish vaqti
- pKmen: ning o'lchovi ligandni bog'lash qarindoshlik
Metilnaltrekson bromidi og'iz orqali qabul qilishning biologik etishmovchiligiga ega va shu sababli u har kuni qo'llaniladi teri ostiga. Dozaning qariyb yarmi siydik bilan va biroz kamroq najas bilan chiqariladi, 85% o'zgarishsiz chiqariladi.[24]
Alvimopan yuqori bo'lganligi sababli juda past bioavailability (6%) mavjud majburiy yaqinlik va past ajralish darajasi. Aslida, alvimopan vositachilik qiladi safro sekretsiyasi o'rtacha plazma klirensi 400 ml / min. Metabolizm alvimopan orqali ichak florasi ni natijasida gidroliz alvimopanning faol amid metabolitiga (ADL 08-0011). Shu bilan birga, metabolit past majburiy yaqinligi tufayli klinik jihatdan ahamiyatsiz hisoblanadi.[25]
Naloksegolga yog'li ovqat berilganda, singdirish ortadi. Tozalash asosan orqali jigar metabolizmi (P450-CYP3A) metabolitlarning noma'lum harakatlari bilan. Naloxegol tomonidan yo'q qilingan kichik bo'laklar mavjud buyrak orqali chiqarilishi.[30]
Naldemedin metabolitlari asosan orqali CYP3A nor-naldemedin, u ham metabolitlar orqali UDP-glyukuronosiltransferaza 1A3 dan naldemedine 3-G gacha, ammo kamroq darajada. Ushbu metabolitlar ikkalasi ham opioid retseptorlari antagonistlari, ammo ularnikidan kam kuchliroqdir ota birikma.[35]
Rivojlanayotgan PAMORAlar

Akselopran Theravane Biopharma tomonidan ishlab chiqilgan og'zaki PAMORA. II bosqichni yakunladi klinik sinovlar OIC bilan kasallangan 400 dan ortiq bemorlarda. Axelopran boshqa PAMORA lardan farqli kimyoviy tuzilishga ega, ammo shunga o'xshash ta'sir mexanizmi. U MOR, KOR va DOR uchun antagonist vazifasini bajaradi, ammo DORga qaraganda MOR va KORga nisbatan yaqinligi yuqori. Boshqa PAMORAlar singari, asosiy maqsad IHTni davolashdir.[36]Akselopran, shuningdek, belgilangan dozali kombinatsiyada (FDK) tekshirilmoqda oksikodon. Akselopran va boshqariladigan relefli oksikodonning FDKini yaratish uchun buzadigan amallar bilan qoplash texnologiyasi yordamida amalga oshiriladi.[37]
Retseptorni optimallashtirishga talab mavjud selektivlik va yaqinlik, ularning nomzod birikmalarini o'rganish bilan birga ma'muriy yo'l. Bular giyohvand moddalarni kashf qilish va PAMORAni rivojlantirishning asosiy maqsadlari va kelajakdagi strategiyalaridir, asosan, MORlar funktsional selektiv agonizmni namoyish etadi. Shuning uchun Iqtisodiy Hamjamiyatni maqsad qilgan kelajakdagi nomzod birikmalari optimallashtirilgan selektiv va yaqinlikka ega bo'lgan PAMORAlardir.[27]
Adabiyotlar
- ^ Floettmann, Eike; Bui, Xanx; Sostek, Mark; Payza, Kamol; Eldon, Maykl (2017 yil may). "Opioid kelib chiqadigan ich qotishma davolash uchun periferik ta'sir qiluvchi b-opioid retseptorlari antagonisti Naloksegolning farmakologik profili". Farmakologiya va eksperimental terapiya jurnali. 361 (2): 280–291. doi:10.1124 / jpet.116.239061. PMC 5399635. PMID 28336575.
- ^ Sizar, Omeed; Gupta, Mohit (2019). "Opioidni keltirib chiqaradigan ich qotishi". Milliy biotexnologiya markazi. StatPearls nashriyoti. PMID 29630236. Olingan 4 iyun 2019.
- ^ Bui, Xanx; Chjou, Diansong; Xu, Xongmey; Floettmann, Eike; Al-Xuniti, Nidal (2017 yil iyun). "Periferik ta'sir qiluvchi b-opioid retseptorlari antagonisti Naloksegolning klinik farmakokinetikasi va farmakodinamikasi". Klinik farmakokinetikasi. 56 (6): 573–582. doi:10.1007 / s40262-016-0479-z. PMID 28035588. S2CID 3458268.
- ^ "Chikago universitetida ishlab chiqarilgan dori FDA tomonidan tasdiqlandi". Chikago universiteti yangiliklari. Chikago universiteti yangiliklari. Olingan 30 aprel 2008.
- ^ a b v d Kerol, F. Ayvi; Dolle, Roland E. (2014). "Sof opioid retseptorlari antagonistlarining N-o'rnini bosuvchi trans-3,4-dimetil-4- (3'-gidroksifenil) piperidin sinfini topish va rivojlantirish". ChemMedChem. 9 (8): 1638–1654. doi:10.1002 / cmdc.201402142. ISSN 1860-7187. PMC 5588862. PMID 24981721.
- ^ Zimmerman, Dennis M.; Nikander, Rodni; Xorng, Jong S .; Vong, Devid T. (1978 yil sentyabr). "4-fenilpiperidin seriyasida aniqlangan giyohvand antagonistlari uchun yangi tarkibiy tushunchalar". Tabiat. Qayta nashr etish va ruxsatnomalar. 275 (5678): 332–334. Bibcode:1978 yil natur.275..332Z. doi:10.1038 / 275332a0. PMID 692714. S2CID 4149532.
- ^ "Dori-darmonlarni tasdiqlash to'plami: Entereg (Alvinopan) kapsulalari 21775". www.accessdata.fda.gov. FDA. Olingan 18 iyul 2008.
- ^ Krokett, Set D. Greer, Katarina B.; Heidelbaugh, Joel J.; Falck-Ytter, Yngve; Xanson, Brayan J.; Sulton, Shahnaz (2019 yil yanvar). "Amerika Gastroenterologik Assotsiatsiyasi Instituti tomonidan opioid ta'siridagi ich qotishining tibbiy boshqaruvi bo'yicha qo'llanma". Gastroenterologiya. 156 (1): 218–226. doi:10.1053 / j.gastro.2018.07.016. PMID 30340754.
- ^ "Dori-darmonlarni tasdiqlash to'plami: MOVANTIC (naloxegol) tabletkalari". www.accessdata.fda.gov. FDA.
- ^ "Symproic (naldemedine) tabletkalari". www.accessdata.fda.gov. FDA. Olingan 4 may 2017.
- ^ Streicher, Jon M.; Bilskiy, Edvard J. (2017-09-25). "Opioid bilan bog'liq yon ta'sirlarni davolash uchun periferik ta'sir qiluvchi m-opioid retseptorlari antagonistlari: ta'sir mexanizmi va klinik ta'siri". Farmatsiya amaliyoti jurnali. 31 (6): 658–669. doi:10.1177/0897190017732263. ISSN 0897-1900. PMC 6291905. PMID 28946783.
- ^ Brok, Kristina; Olesen, Syoren Schou; Olesen, Anne Estrup; Frokyaer, Yens Brondum; Andresen, Trin; Drues, Asbyorn Mox (2012-10-01). "Opioid bilan bog'liq ichak disfunktsiyasi". Giyohvand moddalar. 72 (14): 1847–1865. doi:10.2165/11634970-000000000-00000. ISSN 1179-1950. PMID 22950533. S2CID 173168.
- ^ a b Tomas, Jey (2008). "Opioid ta'sirida ichak disfunktsiyasi". Og'riq va simptomlarni boshqarish jurnali. 35 (1): 103–113. doi:10.1016 / j.jpainsymman.2007.01.017. ISSN 0885-3924. PMID 17981003.
- ^ Gelardini, Karla; Di Sesare Mannelli, Lorenso; Byanki, Enrika (2015). "Opioidlarning farmakologik asoslari". Mineral va suyak metabolizmidagi klinik holatlar. 12 (3): 219–221. doi:10.11138 / ccmbm / 2015.12.3.219. ISSN 1724-8914. PMC 4708964. PMID 26811699.
- ^ Torres, Daniele; Parrinello, Gaspar; Trapanese, Katerina; Licata, Juzeppe (2017). "Xoletsistektomiya qilingan bemorda paratsetamol / kodeinning past dozasidan so'ng to'satdan kuchli qorin og'rig'i: voqea xulosasidan o'rganish". Amerika terapiya jurnali. 17 (4): e133-134. doi:10.1097 / MJT.0b013e3181baf253. ISSN 1536-3686. PMID 19829093.
- ^ Brok, Kristina; Olesen, Syoren Schou; Olesen, Anne Estrup; Frokyaer, Yens Brondum; Andresen, Trin; Drues, Asbyorn Mox (2012-10-01). "Opioid bilan bog'liq ichak disfunktsiyasi: patofiziologiya va boshqarish". Giyohvand moddalar. 72 (14): 1847–1865. doi:10.2165/11634970-000000000-00000. ISSN 1179-1950. PMID 22950533. S2CID 173168.
- ^ a b Kaserer, Tereza; Lantero, Akvilino; Shmidhammer, Helmut; Spetea, Mariana; Shuster, Daniela (2016 yil 18-fevral). "m Opioid retseptorlari: yangi antagonistlar va strukturaviy modellashtirish". Ilmiy ma'ruzalar. 6: 21548. Bibcode:2016 yil NatSR ... 621548K. doi:10.1038 / srep21548. ISSN 2045-2322. PMC 4757823. PMID 26888328.
- ^ DeRuiter, Jek (2000). Giyohvand moddalarni iste'mol qilish tamoyillari (PDF). Auburn Education.
- ^ Xaddu, Tanila Ben; Beni, Sabollar; Xostafi, Shandor; Malfacini, Davide; Kalo, Girolamo; Shmidhammer, Helmut; Spetea, Mariana (2014 yil 11-iyun). "Morfin va oksimorfondagi N-o'rnini bosuvchi o'zgarishni farmakologik tekshirishlari: opioid retseptorlari bilan bog'lanish, signalizatsiya va antinotsitseptiv faollik". PLOS ONE. 9 (6): e99231. Bibcode:2014PLoSO ... 999231B. doi:10.1371 / journal.pone.0099231. ISSN 1932-6203. PMC 4053365. PMID 24919067.
- ^ Truong, Phong M.; Xasan, Serxio A.; Li, Yong-Sok; Kopaytik, Tereza A.; Kats, Jonathan L.; Chadderdon, Aaron M.; Traynor, Jon R.; Desham, Jefri R.; Jeykobson, Artur E .; Rays, Kenner C. (2017 yil 15-aprel). "9-gidroksi-5- (3-gidroksifenil) morfanni N-almashtirish bilan opioid retseptorlari yaqinligi va samaradorligini modulyatsiya qilish: sintez va kompyuter simulyatsiyasi". Bioorganik va tibbiy kimyo. 25 (8): 2406–2422. doi:10.1016 / j.bmc.2017.02.064. ISSN 0968-0896. PMC 5407189. PMID 28314512.
- ^ Kavamura, N .; Kataoka, T .; Imay, E .; Ivamura, T .; Xori, M .; Niva, M.; Nozaki, M .; Fujimura, H. (1981 yil 1-yanvar). "Ba'zi bir N-o'rnini bosadigan benzomorfanlarning antagonist-agonist faoliyati". Endogen va ekzogen opioidlarning yutuqlari. Elsevier: 411-413. doi:10.1016 / B978-0-444-80402-0.50138-8. ISBN 9780444804020.
- ^ a b Manglik, Aashish; Kruse, Endryu S.; Kobilka, Tong Sun; Tyan, Fun Sun; Mathiesen, Jesper M.; Sunaxara, Rojer K.; Pardo, Leonardo; Vays, Uilyam I.; Kobilka, Brayan K.; Granier, Sebastien (2012 yil may). "Morfinan antagonisti bilan bog'langan b-opioid retseptorlari kristalli tuzilishi". Tabiat. 485 (7398): 321–326. Bibcode:2012 yil natur.485..321M. doi:10.1038 / nature10954. ISSN 1476-4687. PMC 3523197. PMID 22437502.
- ^ a b "Metilnaltrekson bromidi". pubchem.ncbi.nlm.nih.gov.
- ^ a b R. Uilyam, Xipkin; Dolle, Roland E. (2010). "9-bob - oshqozon-ichak traktining buzilishi uchun opioid retseptorlari antagonistlari". Tibbiy kimyo bo'yicha yillik hisobotlar. 45: 142–155. doi:10.1016 / S0065-7743 (10) 45009-5.
- ^ a b Zabirovich, Erik S.; Gan, Tong J. (2019). 34 - Operatsiyadan keyingi ko'ngil aynish va gijjalar farmakologiyasi. Elsevier. 671-692 betlar. doi:10.1016 / B978-0-323-48110-6.00034-X. ISBN 9780323481106.
- ^ a b "Naloxegol". pubchem.ncbi.nlm.nih.gov.
- ^ a b Streicher, Jon M.; Bilskiy, Edvard J. (dekabr 2018). "Opioid bilan bog'liq yon ta'sirlarni davolash uchun periferik ta'sir qiluvchi m-opioid retseptorlari antagonistlari: ta'sir mexanizmi va klinik ta'siri". Farmatsiya amaliyoti jurnali. 31 (6): 658–669. doi:10.1177/0897190017732263. ISSN 0897-1900. PMC 6291905. PMID 28946783.
- ^ Xu, Kennet; Bridgeman, Meri Barna (2018 yil oktyabr). "Opioid kelib chiqadigan ich qotib qolishni davolash uchun naldemedin (simproik)". Farmatsiya va terapiya. 43 (10): 601–627. ISSN 1052-1372. PMC 6152697. PMID 30271103.
- ^ Inagaki, Masanao; Kume, Masaharu; Tamura, Yoshinori; Xara, Shinichiro; Goto, Yoshihisa; Xaga, Nobuxiro; Xasegava, Tsuyoshi; Nakamura, Takashi; Koike, Katsumi; Oonishi, Shuuichi; Kanemasa, Toshiyuki; Kay, Xiroyuki (2019 yil 1-yanvar). "Naldemedinning kashf etilishi: opioid ta'siridagi nojo'ya ta'sirlarni davolash uchun kuchli va og'iz orqali qabul qilinadigan opioid retseptorlari antagonisti". Bioorganik va tibbiy kimyo xatlari. 29 (1): 73–77. doi:10.1016 / j.bmcl.2018.11.007. ISSN 0960-894X. PMID 30446313.
- ^ a b Turon, Alparslon; Saasuh, Vael; Hovsepyan, Karen; Siz, Jing. "Oral Naloxegolning yordamchi ta'siri (Movantik)" (PDF). Clinicaltrials.gov.
- ^ "Alvimopan (ADL 8-2698) | Opioid retseptorlari antagonisti | MedChemExpress". MedchemExpress.com.
- ^ "Metilnaltrekson bromidi". pubchem.ncbi.nlm.nih.gov.
- ^ Kanemasa, Toshiyuki; Koike, Katsumi; Aray, Toxo; Ono, Xiroko; Xorita, Narumi; Chiba, Xiroki; Nakamura, Atsushi; Morioka, Yasuxide; Kixara, Tsuyoshi; Xasegava, Minoru (2019 yil 1-may). "Opioid bilan indikatsiya qilingan ich qotishining in vitro va in vivo modellarida periferik ta'sir qiluvchi m m opioid retseptorlari antagonisti naldemedinning farmakologik ta'siri". Neyroxastroenterologiya va harakatchanlik. 31 (5): e13563. doi:10.1111 / nmo.13563. ISSN 1365-2982. PMC 6850587. PMID 30821019.
- ^ "Opioid retseptorlari | kappa, mu Opioid retseptorlari". www.selleckchem.com. Olingan 2019-10-10.
- ^ Markxem, Entoni (2017 yil may). "Naldemedine: Birinchi global tasdiqlash". Giyohvand moddalar. 77 (8): 923–927. doi:10.1007 / s40265-017-0750-0. PMID 28466424. S2CID 19271743.
- ^ Panemanlar, Yasper; Vanuytsel, Tim; Tack, yanvar (oktyabr 2018). "Opioid sababli oshqozon-ichak simptomlarini davolashda yangi o'zgarishlar". Birlashgan Evropa Gastroenterologiya jurnali. 6 (8): 1126–1135. doi:10.1177/2050640618796748. PMC 6169055. PMID 30288274.
- ^ "Theravance Biopharma: Dasturlar | Oshqozon-ichak harakatining buzilishi". SAYT.