Talliy (I) sulfat - Thallium(I) sulfate
 | |
| Ismlar | |
|---|---|
| Boshqa ismlar Tallous sulfat, talliy sulfat | |
| Identifikatorlar | |
3D model (JSmol ) | |
| ChemSpider | |
| ECHA ma'lumot kartasi | 100.028.365 |
| KEGG | |
PubChem CID | |
| UNII | |
CompTox boshqaruv paneli (EPA) | |
| |
| |
| Xususiyatlari | |
| Tl2SO4 | |
| Molyar massa | 504,83 g / mol |
| Tashqi ko'rinish | oq prizmalar yoki zich oq kukun |
| Hidi | hidsiz |
| Zichlik | 6,77 g / sm3 |
| Erish nuqtasi | 632 ° C (1,170 ° F; 905 K) |
| 2.70 g / 100 ml (0 ° C) 4.87 g / 100 ml (20 ° C) 18,45 g / 100 ml (100 ° C) | |
| −112.6·10−6 sm3/ mol | |
Sinishi ko'rsatkichi (nD.) | 1.860 |
| Tuzilishi | |
| romboid | |
| Xavf | |
| R-iboralar (eskirgan) | R28, R38, R48 / 25, R51 / 53 |
| S-iboralar (eskirgan) | (S1 / 2), S13, S36 / 37, S45, S61 |
| NFPA 704 (olov olmos) | |
| O'lim dozasi yoki konsentratsiyasi (LD, LC): | |
LD50 (o'rtacha doz ) | 16 mg / kg (kalamush, og'iz orqali) 23,5 mg / kg (sichqoncha, og'iz orqali)[1] |
Boshqacha ko'rsatilmagan hollar bundan mustasno, ulardagi materiallar uchun ma'lumotlar keltirilgan standart holat (25 ° C [77 ° F], 100 kPa da). | |
| Infobox ma'lumotnomalari | |
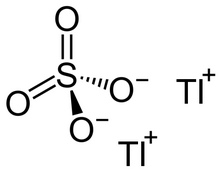
Talliy (I) sulfat (Tl2SO4) yoki tallous sulfat bo'ladi sulfat tuzi talliy Rim raqamlari I. tomonidan ko'rsatilgandek, umumiy +1 oksidlanish holatida, uni ko'pincha oddiy talliyum sulfat deb atashadi.[2]
Foydalanadi
So'nggi ikki asr davomida Tl2SO4 turli xil tibbiy muolajalar uchun ishlatilgan, ammo tashlab yuborilgan. Keyinchalik 1900-yillarda u asosan foydalanishni topdi rodentitsidlar.[3] Ushbu dasturlar 1975 yilda AQShda uning toksikligi tanlanmaganligi sababli taqiqlangan. Talliy (I) sulfat o'simliklarning o'sishini oldini olish orqali inhibe qiladi nihol. Tl2SO4 bugungi kunda asosan Tl manbai sifatida ishlatiladi+ tadqiqot laboratoriyasida. Bu kashshof talliy (I) sulfid (Tl.)2Ta'sir qilganda yuqori elektr o'tkazuvchanligini ko'rsatadigan S) infraqizil yorug'lik.
Tayyorgarlik
Talliy (I) sulfat talliy metalining bilan reaktsiyasi natijasida hosil bo'ladi sulfat kislota dan so'ng kristallanish.
Tuzilishi
Tl2SO4 K bilan bir xil tuzilmani qabul qiladi2SO4. Suvli eritmada talliy (I) kationlar va sulfat anionlar ajratilgan va yuqori darajada solvatlangan. Talliy (I) sulfat kristallari C ga ega2 simmetriya.
Toksiklik
Talliy (I) sulfat suvda eriydi va uning toksik ta'siri talliy (I) kationidan olinadi. Voyaga etgan odam uchun talliy (I) sulfatning o'ldiradigan o'rtacha dozasi taxminan 1 grammni tashkil qiladi. Talliy (I) sulfat noaniq xususiyatlarga ega oddiy kukun bo'lganligi sababli uni zararsiz kimyoviy moddalar bilan osonlikcha adashtirish mumkin. U yutish, nafas olish yoki teriga tegish orqali tanaga kirishi mumkin. Talliy (I) kationi juda o'xshash kaliy va natriy hayot uchun zarur bo'lgan kationlar. Talliy ioni hujayraga kirgandan so'ng, ko'plab jarayonlar kaliy va natriyni tashish buzilgan. Zaharli tabiati tufayli ko'plab g'arbiy mamlakatlar talliy (I) sulfatdan uy sharoitida foydalanish uchun mahsulotlarda foydalanishni taqiqlashdi va ko'plab kompaniyalar ham ushbu birikmani ishlatishni to'xtatdilar.
500 mg dan ortiq dozada o'limga olib keladigan xabar beriladi. Talliy (I) sulfat, tanaga kirgandan so'ng, buyraklar, jigar, miya va tanadagi boshqa to'qimalarda to'planadi.
Talliy (I) sulfat ishlatilgan Isroil kemiruvchilar populyatsiyasini nazorat qilish; 50-yillarda bu yo'qolishiga olib kelgan deb gumon qilinmoqda jigarrang baliq boyo'g'li.[4]
Manbalar
Adabiyotlar
- ^ "Talliy (eruvchan birikmalar, Tl kabi)". Darhol hayot va sog'liq uchun kontsentratsiyalar xavfli (IDLH). Mehnatni muhofaza qilish milliy instituti (NIOSH).
- ^ Mikki, Geynrix; Bo'ri, Xans Uve (2000). "Talliy va talliy birikmalari". Ullmannning Sanoat kimyosi ensiklopediyasi. Vaynxaym: Vili-VCH. doi:10.1002 / 14356007.a26_607.
- ^ Jahon sog'liqni saqlash tashkiloti pestitsidlar №10 (1975)
- ^ Mendelson, H. Isroilda kemiruvchilar va shoqollarni kimyoviy nazorat qilishning ekologik ta'siri LPO Mission Rapaces-da
Tashqi havolalar
- Xalqaro kimyoviy xavfsizlik kartasi 0336
- Kimyoviy xavf-xatarlarga qarshi NIOSH cho'ntagiga oid qo'llanma
- Pestitsidlar to'g'risidagi ma'lumotlar varag'i (JSSV /FAO )
- Kaunas Texnologiya Universiteti
- Viskonsin universiteti-Medison kimyo bo'limi
- Smithsonian National Zoological Park
- IShID jonli qurbonlarga kimyoviy qurollarni sinovdan o'tkazmoqda

